
题目列表(包括答案和解析)
3.在室温时,pH=12的某溶液中,由水电离出的c (OH-)为( )
A.1.0×10-7 mol/L B.1.0×10-2 mol/L
C.1.0×10-12 mol/L D.1.0×10-6 mol/L
2.为使Na2S溶液中c (Na+)/c (S2-)的比值变小,可加入的物质是( )
A.适量NaOH B.适量盐酸 C.适量NaHS D.适量KHS
1.中和10 mL 0.1 mol/L H2SO4溶液,需电离度为2%的氨水40 mL,则氨水的pH为( )
A.3 B.9 C.10 D.11
25.已知:2Fe2+ + Br2 = 2Fe3+ + 2Br-。向100 mL FeBr2 溶液中缓慢通入2.24 L Cl2 (标准状况下),反应结束后溶液中有1/3的Br-被氧化成Br2 。求原FeBr2溶液的物质的量浓度。
24.铝粉与过氧化钠的混合物放入烧杯中加足量水,当反应停止后,变成澄清溶液,测得混合物总质量减少3.5g,再向所得澄清溶液中滴加3.5mol/L的盐酸200mL时,原澄清溶液先无明显现象,后出现白色沉淀,最后又恰好溶解。求原混合物中铝和过氧化钠各多少克?
23.我国在春秋战国时期就懂得将白口铁经退火处理得相当于铸钢的物器(如锋利的刀剑),这一技术要比欧洲早近千年。白口铁退火热处理的主要作用是 。
22.水的硬度表示方法是:将水中的Ca2+、Mg2+折算成CaO的质量,1L水含10 mg CaO为1°。测知5000 kg某净化后的天然水煮沸后冷却得237 g沉淀,冷却水中含MgSO4为840 g,含CaCl2为777 g。将沉淀溶于盐酸得33.6 L CO2(标准状况下)。此天然水的硬度大约是 。
21.下列五个图中,横坐标为向某溶液中加入某物质的量,纵坐标为生成沉淀的量;从A~E中选择符合表中各题要求的序号填在表中。
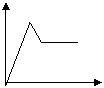
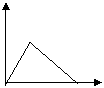
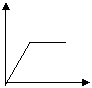
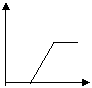
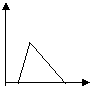
A B C D E
|
溶液 |
加入的物质 |
答案序号 |
|
饱和石灰水 |
通过量CO2 |
|
|
AlCl3溶液 |
通过量NH3 |
|
|
含少量NaOH的NaAlO2溶液 |
通过量CO2 |
|
|
含少量NaOH的NaAlO2溶液 |
逐滴加稀盐酸 |
|
|
MgCl2、AlCl3混合溶液 |
逐滴加NaOH溶液至过量 |
|
|
NaOH溶液 |
逐滴加AlCl3溶液至过量 |
|
20.砖瓦是用含铁元素等杂质的粒土隔绝空气烧制而成的,当烧窑作业临近结束时,若用淋洒水的办法来降低温度,窑内处于还原性气氛,砖块中的铁以氧化亚铁的形式存在,因而砖呈青色。若用捅开窑顶自然冷却的办法,砖就变成了红色。
(1)从化学角度看,砖瓦呈红色的原因是 。
(2)现有一块红砖,实验台上有浓硫酸、3mol/L的盐酸、0.1mol/L硫氰化钾溶液、0.1mol/L氯化铁溶液、0.001mol/L氢氧化钠溶液、蒸馏水等试剂,请选用中学化学常用仪器,设计一个实验,用最简捷的方法验证红砖中含有三价铁。(简述实验步骤、所用仪器、产生现象、所得结论)
。
19.一定条件下,普通铁粉和水蒸气反应可得到铁的氧化物,该氧化物又可以经过此反应的逆反应生成颗粒很小的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热会燃烧,俗称“引火铁”。请分别用图中示意的两套仪器装置,制取上述的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其它试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去)。
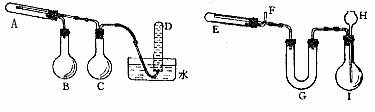
填写下列空白:
(1)实验进行时,试管A中应加入的试剂是 。
烧瓶B的作用是 。
烧瓶C的作用是 。
试管D中收集到的物质是 。
(2)实验时,U型管G中加入的试剂是 。
H中应加入 。
(3)两套装置中,需加热的仪器是(填对应字母) 。
(4)E中反应的化学方程式为 ;为了安全,在E中反应前,在F出口必须 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com