
题目列表(包括答案和解析)
1.下列物质使用不合理的是
A、用白磷制安全火柴 B、液氨作致冷剂
C、明矾用作工业用水的净水剂 D、金的合金用于制造笔尖材料
26、(8分)将0.2mol 金属R的一种含氧酸盐在隔绝空气的条件下加热,使之完全分解,生成R的氧化物RO和CO、CO2的混合气体。已知:该混合气体对氢气的相对密度为18,其体积为8.96L(标准状况);金属R的原子核中质子数比中子数少4。测得RO的质量比原含氧酸盐质量减轻一半。通过计算,求出该盐的化学式。
25、(6分)某气态烃含C 85.7%,含H 14.3%,在标准状况下的密度是2.5g/L。该烃能使酸性高锰酸钾溶液或溴水褪色。求该烃的分子式,并写出它的各种同分异构体的结构简式。
24、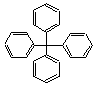 (6分)(1)甲烷分子中的4个氢原子全部被苯基取代,可得如图
(6分)(1)甲烷分子中的4个氢原子全部被苯基取代,可得如图
所示的分子, 该分子中共平面的C原子最多有 个,
共平面的原子最多有 个。
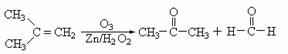 (2)在有机化学分析中,根据反应的性质和反应产物,即可确定烯烃的组成和结构(双键及支链的位置),例如:
(2)在有机化学分析中,根据反应的性质和反应产物,即可确定烯烃的组成和结构(双键及支链的位置),例如:
据以上线索和下列反应事实,确定C7H14的结构和名称:
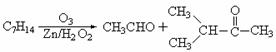 该烃的结构简式是_________________
该烃的结构简式是_________________
23、(12分)甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等。已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子。
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是:
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:
(3)在一定条件下,甲与O2反应的化学方程式是:
(4)丁的元素符号是 ,它的原子结构示意图为 。
(5)丁的氧化物的晶体结构与 的晶体结构相似。
22、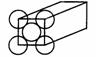 (4分)金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10
m,求
(4分)金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10
m,求
(1)金晶体中最小的一个立方体含有__________个金属原子。
(2)金的密度为_________g·cm-3。
21、(8分)A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、
E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。D、A按原子个数比3∶2形成离子化合物丙。E是地壳中含量最高的金属元素。根据以上信息回答下列问题: (1)B元素在周期表中的位置是___________,乙物质的电子式是____________。 (2)A、B、C、D、E五种元素的原子半径由小到大的顺序是_____ _(用元素符号填写)。 (3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是_____ __。
20、(8分)下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表形成共价键的最外层电子,短线代表价键,如,F2: 。以下四种图式各代表的分子是:
。以下四种图式各代表的分子是:
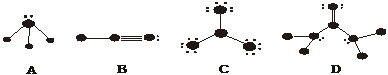
A ,B ,C ,D 。
19、(12分)(1)下列各化合物中,属于同系物的是(填入编号) ,属于同分异构体的是 。
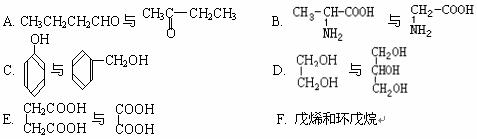
(2) 按系统命名法命名
① 有机物CH3CH(C2H5)CH(CH3)2的名称是________________________.
② 在有机物分子中若某一个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”。C7H16的同分异构体中具有“手性碳原子”的有_______种,名称分别为___________________________________________________________________________
18、 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如右
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如右
图所示,现提供以下化学键的键能(kJ·mol-1)
P-P:198 P-O:360 O=O:498,
则反应P4(白磷)+ 3O2 → P4O6的反应热△H为(化
学反应的△H等于反应中断裂旧化学键的键能之和
与反应中形成新化学键的键能之和的差)( )
A、-1638 kJ/mol B、+1638 kJ/mol
C、-126 kJ/mol D、+126 kJ/mol
Ⅱ卷(64分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com