
题目列表(包括答案和解析)
1.在一个大萝卜中挖一个大孔,向其中注入一定量的饱和食盐水,过一段时间后将里面的食盐水倒出,再往倒出的食盐水中加入少量食盐晶体。则食盐水的质量会( )
A.不变,因为倒出的食盐水还是饱和的
B.增加,倒出的食盐水还是饱和的,但加入了食盐,故溶液的质量增加
C.增加,倒出的食盐水不饱和了,加入的食盐会溶解一部分
D.减少,因为有一部分食盐变成晶体析出
解析:根据生物知识可知,萝卜的水会向饱和食盐水中渗透,使饱和食盐水变得不饱和了,所以还可以继续溶解食盐。
答案:C
8.对某不饱和溶液采取下列措施,有关的量将如何变化?用“增大”“不变”或“减小”填表:
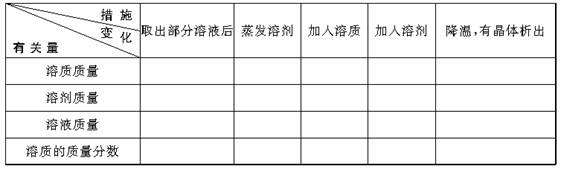
解析:本题的解题依据是:溶液的组成成分,饱和溶液与不饱和溶液的互相转化和溶质质量分数的计算公式。
答案:
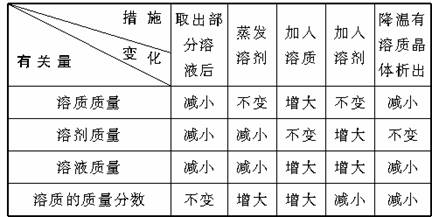
30分钟训练(巩固类训练,可用于课后)
7.经测定KNO3在不同温度时的溶解度数据如下表:
|
温度℃ |
20 |
40 |
60 |
80 |
100 |
|
溶解度/g |
31.6 |
63.9 |
110 |
169 |
246 |
(1)30 ℃时,在盛有100 g水的烧杯中,加入65 g硝酸钾晶体,用玻璃棒搅拌。下列说法中,不正确的是( )
A.所得溶液是不饱和溶液 B.硝酸钾晶体不能全部溶解
C.所得溶液是饱和溶液 D.在所得溶液中还可能溶解其他溶质
(2)在上述所得溶液中加水,或加硝酸钾晶体,或降低温度,或升高温度等四种情况下(其他条件不变),其溶质的质量分数变化趋势不正确的图象是( )
(注:溶液的质量分数是指溶液中的溶质质量占整个溶液总质量的百分比)
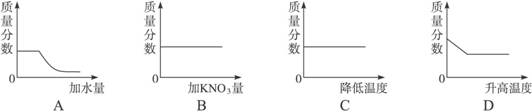
解析:(1)从表中可知,30 ℃时,100 g水中加入65 g KNO3晶体,不能全部溶解,A选项是错误的。(2)硝酸钾在降低温度条件下,其溶解度降低,质量分数减小。注意A、D选项中,加水或升温时,原来未溶解的KNO3继续溶解。
答案:(1)A (2)CD
6.闻名中外的青岛啤酒内溶有一定量的二氧化碳气体,打开瓶塞时,你会发现啤酒会自动喷出来。喝了啤酒后又会常常打嗝,这说明气体在水中的溶解度与压强和温度有关。下列关于气体溶解度的说法正确的是( )
A.压强减小,气体溶解度增大 B.压强减小,气体溶解度减小
C.温度降低,气体溶解度减小 D.气体溶解度与温度无关
解析:打开瓶塞,瓶内压强减小,气体会喷出来,说明溶解度减小;人体内温度更高,喝啤酒后会打嗝,实质上是气体逸出,说明溶解度减小。
答案:B
5.在室温的条件下,试管里盛有一种无色透明的溶液,将试管放入盛有热水的烧杯中,可观察到试管里的溶液变浑浊。下列说法正确的是( )
A.该溶液中的溶质可能是硝酸钾 B.该溶液中的溶质可能是氢氧化钙
C.放入热水前的无色透明溶液一定是饱和溶液 D.变浑浊后的溶液一定是浓溶液
解析:氢氧化钙的溶解度随温度升高而变小,升高温度氢氧化钙会结晶析出而使溶液变浑浊,但由于其溶解度较小,故不是浓溶液。
答案:B
4.t ℃时,有两瓶硝酸钾溶液,一瓶为饱和溶液(溶质的质量占整个溶液质量的40%),另一瓶为溶质的质量占整个溶液质量的10%的溶液,下列实验操作中,无法区分这两种溶液的是( )
A.略降低温度 B.加少量的硝酸钾晶体
C.加一定量的水 D.蒸发少量水后,温度恢复至t ℃
解析:硝酸钾的溶解度随温度降低而减小,饱和溶液略降低温度有硝酸钾晶体析出,不饱和溶液则没有;饱和溶液中加硝酸钾晶体不溶解,而不饱和溶液中硝酸钾晶体会溶解;蒸发少量水后饱和溶液有部分晶体析出,而不饱和溶液则没有。可见,A、B、D方法可以区分这两种溶液,C方法则无法区分。
答案:C
3.某温度下,A物质的溶解度为S克,则它的饱和溶液的溶质在整个溶液中的质量分数是( )
A.大于S% B.小于S% C.等于S% D.无法判断
解析:根据溶解度的定义,可知饱和溶液的质量分数等于?S/(100+S),应该比S?%小。
答案:B
2.室温下,向一定质量的氯化钠溶液中加入10 g 氯化钠固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解。下列判断正确的是( )
A.加水后一定是不饱和溶液 B.加水前可能是饱和溶液
C.加水后一定是饱和溶液 D.加水前一定是饱和溶液
解析:加水前,该溶液一定是饱和溶液,因为有固体剩余;加水后固体全部溶解,有可能是饱和溶液了,也有可能是不饱和溶液。
答案:D
1.若要从饱和的氯化钠溶液中获得较多的晶体,下列方法中,你认为最合理的是( )
A.升高溶液的温度 B.蒸发溶剂
C.降低溶液的温度 D.从溶液中倒掉一部分水
解析:氯化钠的溶解度受温度变化影响大,应用蒸发溶剂的方法能获得较多的晶体。
答案:B
4.下列说法是否正确?正确的,在( )中打“√”,错误的,在( )中打“×”。
(1)100 g水溶解了30 g某物质,则该物质的溶解度为30 g( )
(2)任何物质的溶解度随温度升高都增大( )
(3)饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液( )
(4)饱和溶液析出晶体后,其溶质在整个溶液中的质量分数一定减小( )
(5)温度相同的条件下,同一种物质的饱和溶液比不饱和溶液溶质的质量分数要大一些( )
解析:(1)没有说明温度,也没有说明溶液是否饱和,所以错误。
(2)大多数物质的溶解度随温度升高而增大,少数物质的溶解度随温度升高而减小,如Ca(OH)2。
(3)判断是饱和溶液,还是不饱和溶液要看在某一温度和一定量溶剂中能否再溶解溶质,而浓、稀溶液是指一定量的溶液中含溶质的数量的多少,所以没有必然的联系。
(4)饱和溶液析出晶体后,还是饱和溶液,溶质的质量分数不变。
(5)温度相同的条件下,相同质量溶剂的同一种物质饱和溶液所含溶质较多,不饱和溶液所含溶质较少。
答案:(1)× (2)× (3)× (4)× (5)√
10分钟训练(强化类训练,可用于课中)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com