
题目列表(包括答案和解析)
13.在含氧酸中有一种称为原某酸的,一般不稳定,易脱水;它与对应的含氧酸的区别在于H、O原子数目的不同。例如:硅酸的化学式H2SiO3,原硅酸的化学式为H4SiO4;碳酸的化学式为H2CO3,原碳酸的化学式为H4CO4,据此可推知,下列结构简式中属于原甲酸乙酯的酯类是
A.C(COC2H5)4 B.CO(OC2H5)2
C.H2C(COC2H5)2 D.HC(OC2H5)3
12.A、B、C为三种短周期元素,A、B在同周期, A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中正确的是
A.原子序数:A>B>C B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
11.聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}加入到被镉离子污染的水体中,利用PFS在水体中形成絮状物,以吸附镉离子,从而减少危害。下列说法中不正确的是
A.10848Cd核素中中子数为60
B.PFS中铁显十2价
C.含镉废电池应进行回收处理
D.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程。
10.在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:
C(s)+H2O (g) CO(g)+H2(g)。
CO(g)+H2(g)。
下列叙述中不能认定上述可逆反应在一定条件下已达到化学平衡状态的是
A.体系的压强不再发生变化
B.v正(CO)=v逆(H2O)
C.生成n molCO的同时生成n mol H2
D.1 mol H-H键断裂的同时断裂2 molH-O键
9.电解NaCl-KCl-AlCl3熔体制铝比电解Al2O3-NaAlF6制铝节省电能约30%,但现在仍用后一种方法制铝,其主要原因是
A.AlCl3是分子晶体,其熔体不导电
B.电解AlCl3生成的Cl2会严重污染大气
C.自然界不存在富含AlCl3的矿石
D.生产无水AlCl3较困难,成本又较高
15. 在某100mL混合酸中, 物质的量浓度为0.4mol/L,
物质的量浓度为0.4mol/L,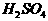 的浓度为
的浓度为 。向其中加入2.56g铜粉,微热,待充分反应后,溶液中
。向其中加入2.56g铜粉,微热,待充分反应后,溶液中 物质的量浓度约为
物质的量浓度约为
A.  B.
B.

C.  D.
无法计算
D.
无法计算
班级______ 姓名__________ 座号_____ 成绩_______
14. 在强酸性溶液中,可以大量共存的离子组是
A. 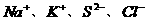 B.
B.
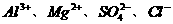
C. 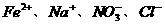 D.
D.
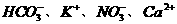
13. 浓硝酸往往显黄色是因为
A. 溶有溴在其中 B.
其中含有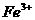
C. 溶有硫黄在其中 D. 溶有自身分解的
12. 某温度下,在体积一定的密闭容器中适量的 (气)和
(气)和 (气)恰好完全反应,若反应产物中只有
(气)恰好完全反应,若反应产物中只有 (气)和
(气)和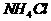 (固),则反应前后容器中压强比应接近于
(固),则反应前后容器中压强比应接近于
A. 7:11 B. 11:7 C. 11:1 D. 1:11
11. 有甲、乙、丙三种气体,甲无色,一定条件下,甲能与氧气反应生成乙;乙不溶于水,但能与氧气进一步反应生成丙;甲、丙皆溶于水,但其水溶液酸碱性恰好相反,则
A. 甲: 乙:
乙: B. 甲:
B. 甲: 乙:
乙:
C. 甲: 丙:
丙: D. 甲:
D. 甲: 乙:
乙:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com