
题目列表(包括答案和解析)
18、炒过菜的铁锅末及时洗净(残液中含NaCl),第二天便会因被腐蚀而出现红棕色锈斑。试回答:(1)、铁锅的铁锈应属于_______腐蚀,腐蚀的原因是________(2)、铁锅腐蚀的电极反应式为:负极:____________正极:____________;正、负电极反应产物会继续发生反应,反应的离子方程式或化学方程式为____________________、_____________、______________.
高二第四章《几种重要的金属》测试题
17、铝片溶于热的烧碱溶液,反应的离子方程式为 ,该反应中氧化剂是 。向反应后的溶液逐滴加入稀盐酸,最初会产生白色沉淀,反应的离子方程为 。
16、把等物质的量的Cu、Fe投入一定量的FeCl3溶液中充分反应后,若溶液呈蓝色,加入KSCN溶液不显血红色,那么溶液里存在的金属离子有:______可能存在的金属粉末物质是:______。
15、agMg在盛有bL(标况)CO2 和O2混合气的密闭容器中燃烧,反应结束后:(1)、若反应容器中的气体只有CO2,则容器内的固体一定含:______;(2)若反应容器中的气体中仍有O2剩余,则容器内的固体质量为:________g;(3)、若反应容器中无气体剩余,则容器内固体物质质量(m)的取值范围:______________________________。
14、有A、B、C、D、E、F、G七种物质,它们的变化关系如下图所示:
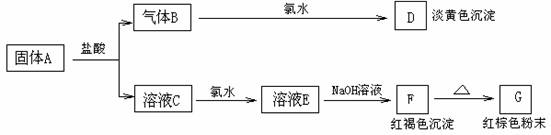
(1)写出下列物质化学式:A F G ;
(2)写出下列变化的化学方程式:
B→D: ; C→E: ;
13、在含有少量盐酸的AlCl3溶液中逐滴加入过量的氨水至溶液呈碱性,下列图中,能表示该反应产生的沉淀的质量W与加入氨水的何积V关系的是( )

12、电子表和计算器的电源是微型银锌原电池,其电极材料分别为Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn + 2OH- - 2e- = ZnO+ H2O, Ag2O+ H2O +2e- = 2Ag + 2OH-,下列说法不正确的是 ( )
A. Zn为正极,Ag2O为负极 B.电子由锌经外电路流入Ag2O极
C. Zn为负极,Ag2O为正极 D.工作一段时间后,Zn质量减少
11、由Na、Mg、Al、Fe四种金属中的两种组成的混合物12g,与足量的盐酸反应产生氢气0.5g,则混合物中一定含有的金属是( )
A、Na B、Mg C、Al D、Fe
10、下列实验装置中,一段时间后原电池正极会增重的是()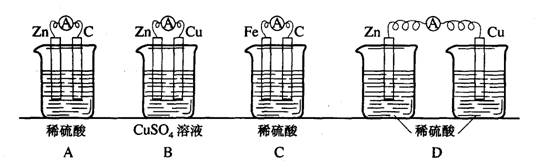
9、将5.6g铁粉加入0.3mol硝酸铁的溶液中,充分反应后( )
A、Fe3+全部被还原 B、Fe3+部分被还原,Fe全部被氧化
C、Fe部分被氧化 D、溶液中只有Fe2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com