
题目列表(包括答案和解析)
6.将①H+ ②Cl- ③Al3+ ④K+ ⑤O2-五种微粒分别加入水中,基本上不影响水的电离平衡的有( )
A.①②④⑤ B.②④⑤ C.①③⑤ D.②④
5.在含有下列离子的各100ml溶液中,无论是加酸还是加碱(不考虑溶液体积变化),都能使这种离子浓度减小的是( )
A. 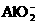 B.
B.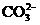 C.
C.
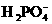 D.NH+4
D.NH+4
4.下列物质溶于水,由于水解而使溶液显酸性的是( )
A.P2O5 B.NaHSO4 C.CuCl2 D.NaF
3.确定酸溶液的酸性强弱的根据是( )
A.酸的强弱 B.酸分子中可电离出的H+个数
C.酸浓度 D.c(H+)
2.下列关于混合物,纯净物,强电解质,弱电解质和非电解质的正确组合是( )
|
|
纯净物 |
混合物 |
强电解质 |
弱电解质 |
非电解质 |
|
A |
纯盐酸 |
水煤气 |
硫酸 |
醋酸 |
干冰 |
|
B |
冰醋酸 |
空气 |
硫酸钡 |
亚硫酸 |
二氧化硫 |
|
C |
氯气 |
盐酸 |
苛性钠 |
氢硫酸 |
碳酸钙 |
|
D |
重钙 |
普钙 |
氯化钠 |
次氯酸 |
氯气 |
1.在任何一种电解质溶液中,下列说法正确的是( )
A.阴、阳离子总数相等 B.阴、阳离子所带的电荷数相等
C.都存在未电离的溶质分子 D.溶液呈电中性
35.(8分)向100 mL某二价金属M的氢氧化物澄清溶液中加入过量的 NaHCO3溶液,生成了MCO3沉淀,过滤,将沉淀置于足量的盐酸溶液中,在标准状况下收集到4.48L气体。将滤液加水稀释至 250 mL,取出 25 mL恰好与 20 mL盐酸完全反应,在标准状况下收集到1.12L气体。
(1)M的氢氧化物澄清溶液与NaHCO3溶液反应的化学方程式为:
___ __。
(2)要计算金属M的原子量,你认为还必须提供下列哪项数据(填写供选项字母序号)____。
(A)M的氢氧化物溶液的物质的量浓度(设为2mol·L-1)
(B)M的碳酸盐的质量(设为39.4 g)
(C)与M的碳酸盐反应的盐酸的物质的量浓度(设为 0.1mol·L-1)
(D)题设条件充足,不需要补充数据。
(3)根据你的选择,试计算金属M的原子量和加入的NaHCO3溶液中所含的NaHCO3的质量。
1999-2000学年度第二学期期末高二化学试卷
34、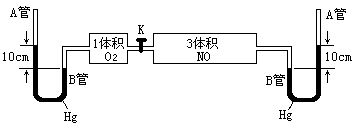 (6分)如图所示,打开两个容器间的活塞K,使两种气体混合,充分反应,达到平衡状态时(温度不变),A管中汞液面比B管中汞液面高7.1cm,(反应开始时高10cm),设此温度
(6分)如图所示,打开两个容器间的活塞K,使两种气体混合,充分反应,达到平衡状态时(温度不变),A管中汞液面比B管中汞液面高7.1cm,(反应开始时高10cm),设此温度
产物为气态,汞蒸汽压忽
略不记,体系容积为定值。
求NO2转化为N2O4的转
化率。
33、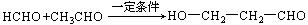 (9分)已知:①乙醛甲基上的氢原子是α氢原子,活性较大,可以与甲醛中的醛基发生加成反应,如:
(9分)已知:①乙醛甲基上的氢原子是α氢原子,活性较大,可以与甲醛中的醛基发生加成反应,如:
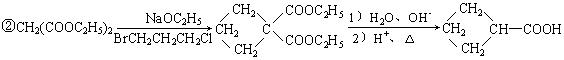 现由乙烯和丙二酸等物质合成I,合成路线如下:
现由乙烯和丙二酸等物质合成I,合成路线如下:
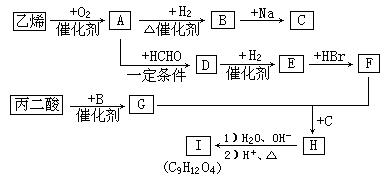
请回答下列问题:
(1)写出下列物质的结构简式:
E 、H
I ;
(2)写出A→D的化学方程式:(有机物写结构简式):
。
32、(8分)某α-氨基酸,分子量不超过200,经分析可知,该氨基酸含C、H、O、N四种元素,其中氮元素的质量分数为8.5%,氧的质量分数为19.4%。
(1)该氨基酸的分子中有 个-NH2, 个-COOH。
(2)该氨基酸分子量(取整数值)为 。
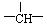 (3)若氨基酸分子结构中无甲基(-CH3),有和苯环,写出其结构
(3)若氨基酸分子结构中无甲基(-CH3),有和苯环,写出其结构
简式 。
(4)另有一种有机物A是上述氨基酸的同分异构体,A分子中也含有苯环,但不含-NH2和-COOH,且苯环上的一卤代物只有一种,则A的结构简式可能
为: 、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com