
题目列表(包括答案和解析)
2.金属冶炼方法的选择
1.金属冶炼的基本原理
3.方法导引
(1)熟练掌握金属活动性顺序表,注重该表在学习中的指导作用.如判断金属元素在自然界的存在形式,金属的还原性以及根据金属的还原性所采取的冶炼方法.
(2)锻炼自学能力,在教师的指导下自学教材内容,归纳金属冶炼的方法并应用到其它金属的冶炼.
[重点难点解析]
重点:工业上冶炼金属的一般方法:热分解法、热还原法、电解法.
难点:不同金属冶炼方法不同.如何选择合适的冶炼方法.
金属冶炼的本质是金属的离子从化合物中被还原成金属单质的过程.从金属活动顺序表可知,越活泼的金属,其阳离子的氧化性越弱;反之,越不活泼的金属,其阳离子的氧化性越强,因此不同的金属冶炼方法也不同.金属的位置越靠后,越容易被还原,用一般的还原方法就能使金属还原;金属的位置越靠前,越难被还原,最活泼的金属只能用最强的还原手段(电解)来还原.
[难题巧解点拨]
例1:某冶炼铝厂以碳棒为电极,电解熔融的三氧化二铝,当生成27kg铝时,阳极消耗12kg碳,则在阳极生成的CO2和CO二种气体的分子个数比为 .
分析 电解法炼铝的反应式为:
2Al2O3 4Al
+ 3O2↑
4Al
+ 3O2↑
(阴极) (阳极)
在高温下,阳极产生的O2,易把石墨电极氧化为CO2和CO.
由题意:阴极产生的铝: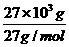 =1×103mol
=1×103mol
阳极消耗的碳: =1×103mol
=1×103mol
而由方程式可算出阳极产生的O2为:
1×103×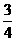 =0.75×103mol.
=0.75×103mol.
阳极消耗的碳与产生的O2即反应生成CO和CO2.设生成的CO2为xmol,CO为ymol.则

解得  故生成CO2和CO的分子个数比为1∶1
故生成CO2和CO的分子个数比为1∶1
例2:为何工业上制镁时用电解MgCl2,而制铝时通常是电解Al2O3?
分析 作为工业生产,一要考虑原料来源、价格,二要考虑生产过程的能源消耗.MgCl2的溶点只有714℃,而MgO为2800℃,从能量消耗上来看显然用MgCl2优于MgO.MgCl2原料可从天然光卤石KCl·MgCl2·6H2O和海水中获得,所以工业上常采用在750℃左右电解无水MgCl2来制镁.而制铝的原料多来自铝土矿(主要成分为Al2O3),Al2O3的熔点也很高,为2045℃,但加入冰晶石(Na3AlF6)作熔剂,则可使Al2O3在962℃即熔化,而使铝得以大量生产.如果用电解AlCl3法,首先把铝土矿制成AlCl3要耗能及设备,且加热AlCl3时,AlCl3易气化,熔融态AlCl3未电离,不导电.
[命题趋势分析]
常考知识点:
2.知识网络

1.金属的冶炼原理是将金属的化合物通过还原的方法使金属离子还原成金属单质.
由于金属的化学活动性不同,金属离子得到电子,还原成金属原子的能力也不同,所以采用不同的冶炼方法.
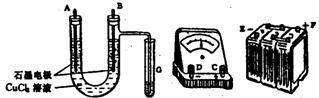
14.(01湖北)某学生试用电解法根据电报上析出的物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:(1)用直流电源电解CuCl2溶液,所用仪器如下图:(2)在电流强度为1安培,通电时间为t秒时,精确测得某电极上析出的Cu的质量为mg。回答:
(1)连接这些仪器的正确顿序为E接 ,C接 , 接F。
实验线路中的电流方向为 → → → → →
(2)写出B极上发生反应的离子方程式
G试管中淀粉K1溶液变化的现象为 ,相应的离子方程式为
(3)为精确测定电极上析出Cu的质量,所必需的实验步骤的先后顺序应是(选填下列操作步骤的编号)
。
①称量电解前电极质量 ②刮下电解后电极上的Cu,并清洗 ③用蒸馏水清洗电解后电极 ④低温烘干电极后称量 ⑤低温烘干刮下的Cu后称量 ⑥再次低温烘干后称量到恒重。
(4)已知电子的电量为1.6×10-19C,试列出阿伏加德罗常数的计算表达式
NA= 。
13.以铂电极电解CuCl2溶液,当电流强度为a安培,通电时间为t分钟,阴极增重W克,在阳极得V L(标况)纯净气体,则阿伏加德罗常数的计算式为(1个电子电量为q库仑,铜的相对原子质量为M) ( )
A.32at/qw B.672at/Vq C.30Mat/qw D.无法列式
12.(99湖北)用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L氧气(标准状况),从而可知M的原子量为
A 22.4ax/b B 11.2ax/b C 5.6ax/b D 2.5ax/b
11.(98贵州)用惰性电极电解CuCl2和Cu(NO3)2的混和溶液(浓度均为0.01mol/L)500mL,当阴极析出0.48克铜时,标准状况下阳极产生的气体体积约为( )
A、0.224L B、0.336L C、0.14L D、0.24L
10.(97浙江)在一定温度下,电解硫酸钾饱和溶液,当阳极产生a摩气体时,溶液中析出W克晶体(不含结晶水),设电解过程中温度保持不变,则剩余溶液的溶质的分数为( )
A. B.
B.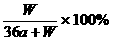 C.
C. D.
D.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com