
题目列表(包括答案和解析)
20、为测定一种复合氧化物开支的磁性粉末材料的组成,称取12.52克样品,将其全部溶于过量稀硝酸后,配成100毫升溶液。取其一半,加入过量K2SO4溶液,生成白色沉淀,经过滤、洗涤、烘干后得4.66克固体。在余下的50毫升溶液中加入少许KSCN溶液,显红色;如果加入过量NaOH溶液,则生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得3.20克固体。(1)计算磁性粉末材料中氧元素的质量百分含量。(2)确定该材料的化学式
19.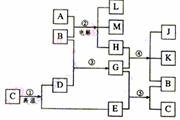 (12分)根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(12分)根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应。
(1)单质L是 ▲ 。
(2)化合物B是 ▲ 。
(3)图中除反应①以外,还有两个用于工业生产的反应,是 ▲ 和 ▲ (填代号)。它们的化学反应方程式分别是 ▲ 和 ▲ 。
18.(10分)A是一种含碳、氢、氧三种元素的有机化合物。已知:A中碳的质量分数为44.1%,氢的质量分数为8.82%;A只含有一种官能团,且每个碳原子上最多只连一个官能团:A能与乙酸发生酯化反应,但不能在两个相邻碳原子上发生消去反应。请填空:
(1)A的分子式是 ▲ ,其结构简式是 ▲ 。
(2)写出A与乙酸反应的化学方程式: ▲ 。
(3)写出所有满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是 ▲ 。
17.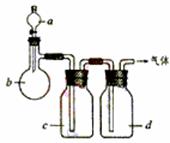 (15分)拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
(15分)拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
|
气体 |
a |
b |
c |
d |
|
C2H4 |
乙醇 |
浓H2SO4 |
NaOH溶液 |
浓H2SO4 |
|
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
|
NH3 |
饱和NH4Cl溶液 |
消石灰 |
H2O |
固体NaOH |
|
NO |
稀HNO3 |
铜屑 |
H2O |
P2O5 |
(1)上述方法中可以得到干燥、纯净的气体是 ▲ 。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体 ▲ ,理由是 ▲ 。
②气体 ▲ ,理由是 ▲ 。
③气体 ▲ ,理由是 ▲ 。
④气体 ▲ ,理由是 ▲ 。
16.(7分)(1)无水乙酸又称冰醋酸(熔点16.6℃)。在室温较低时,无水乙酸就会凝结成像冰一样的晶体。请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。答: ▲
(2)要配制浓度约为2mol·L-1 NaOH溶液100mL,下面的操作正确的是 ▲ (填代号)。
A 称取8g NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
B 称取8g NaOH固体,放入100mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
C 称取8g NaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
D 用100mL量筒量取40mL 5mol·L-1NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
15.人们使用四百万只象鼻虫和它们的215磅粪物,历经30年多时间弄清了棉子象鼻虫的四种信息素的组成,它们的结构可表示如下(括号内表示④的结构简式)
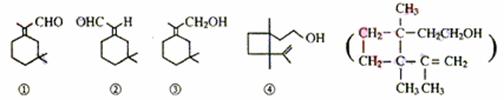
以上四种信息素中互为同分异构体的是
A ①和② B ①和③ C ③和④ D ②和④
第II卷(非选择题,共58分)
14.设NA表示阿伏加德罗常数,下列叙述中正确的是
A 常温常压下,11.2L氧气所含的原子数为NA
B 1.8g的NH4+离子中含有的电子数为NA
C 常温常压下,48gO3含有的氧原子数为3NA
D 2.4g金属镁变为镁离子时失去的电子数为0.1NA
13.能正确表示下列化学反应的离子方程式是
A 用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
B 金属铝溶于盐酸中:Al+2H+=Al3++H2↑
C 硫化钠溶于水中:S2-+2H2O=H2S↑+2OH-
D 碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑
12.对某酸性溶液(可能含有Br-,SO42-,H2SO3,NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是
A Br- B SO42- C H2SO3 D NH4+
11.若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
A Al3+ Na+ NO-3 Cl- B K+ Na+ Cl- NO3-
C K+ Na+ Cl- AlO2- D K+ NH+4 SO42- NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com