
题目列表(包括答案和解析)
1.电导仪测得液态BrF3具有微弱的导电性,表示BrF3(液)中有阴、阳离子X和Y存在.X和Y也存在于BrF2SbF6、KBrF4、(BrF2)2SnF6等化合物中,则X、Y的化学式分别为( )
A.X为F- Y为Br3+ B.X为BrF-4 Y为BrF+2
C.X为F- Y为BrF+2 D.X为BrF-4 Y为Br3+
28.写出下列反应的离子方程式
(1)氨气跟稀H2SO4反应
(2)氢氧化钡溶液跟过量的硫酸氢钠溶液反应
(3)小苏打溶液跟烧碱溶液反应
(4)将SO2通入氯水中的反应
(5)小苏打溶液跟过量澄清石灰水的反应
[素质优化训练]
27.填写下列物质溶于水后的电离方程式:
(1)HI
(2)Ca(OH)2
(3)Fe(OH)3
(4)H2SO3
(5)H3PO4
(6)NaH2PO4
(7)BaSO4
26.在BaCl2溶液中滴加Na2C2O4(草酸钠)溶液,产生白色沉淀.在白色沉淀中加入盐酸,沉淀溶解.
(1)试用离子方程式和有关平衡的知识解释
(2)根据上述判断,可得出酸盐跟反应的一种规律是
25.在MgCl2溶液中加入氨水,能产生白色沉淀等离子方程式为 .
若在MgCl2溶液中先加入大量的固体NH4Cl后再加入氨水,则无沉淀产生,原因是
.
24.金属能导电,是因为存在 ,电解质导电是因为存在 ,液态氯化氢不导电原因是 ,氯化氢的水溶液能导电原因是 .
23.H2S溶液中存在着H2S H++HS-和HS-
H++HS-和HS- H++S2-的平衡.(1)当向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,S2-的物质的量浓度 ,H+的物质的量浓度
(2)当向溶液中加入NaCN,电离平衡向
移动,H+的物质的量浓度
,S2-的物质的量浓度 (3)当向溶液中通入Cl2时,S2-的物质的量浓度 ,H+的物质的量浓度 .
H++S2-的平衡.(1)当向H2S溶液中加入CuSO4溶液时,电离平衡向 移动,S2-的物质的量浓度 ,H+的物质的量浓度
(2)当向溶液中加入NaCN,电离平衡向
移动,H+的物质的量浓度
,S2-的物质的量浓度 (3)当向溶液中通入Cl2时,S2-的物质的量浓度 ,H+的物质的量浓度 .
22.在氯水中存在着 种分子,它们是 ,同时存在着 离子,它们是 .
21.在弱电解质电离过程中,分子电离成离子的速度逐渐 ,同时离子结合成分子的速率则逐渐 ,在一定条件下,当二者速率 时就达到平衡状态.
19.下列溶液均是50ml,若分别向其中加入0.5mol/L盐酸,则溶液的导电性明显增强的是( )
A.0.5mol/L的H2SO4 B.0.5mol/L的NaOH
C.0.5mol/L的NH3·H2O D.0.5mol/L的AgNO3
*20.NH3·H2O的电离平衡常数为:
Kb=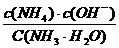
则溶液中各离子和分子的浓度大小为:( )
H+4)=c(OH-)=c(NH3·H2O) H+4)>c(OH-)>c(NH3·H2O)
H+4)=c(OH-)>c(NH3·H2O) H+4)=c(OH-)<c(NH3·H2O)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com