
题目列表(包括答案和解析)
22、 (12分)A-L为中学化学中的常见物质,它们有如图所示转化关系,其中A为坚硬难熔的主族元素的化合物,B为黑色晶体,则
(12分)A-L为中学化学中的常见物质,它们有如图所示转化关系,其中A为坚硬难熔的主族元素的化合物,B为黑色晶体,则


(1)写出物质的化学式
B 、 E 、 H 、K ;
(2)书写反应方程式:
①
②
③
④

21、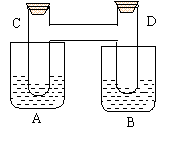 (10分)如图所示在烧杯A、B中均盛有20℃、50mL水,试管C与D相通,其
(10分)如图所示在烧杯A、B中均盛有20℃、50mL水,试管C与D相通,其 中充有红棕色气体,处于下列平衡2NO2
N2O4 (正反应放热)。当向A中加入10g NaOH固体使其溶解,往B中加入50g硝酸铵也使其溶解(20℃时,硝酸铵的溶解度为197g),则:
中充有红棕色气体,处于下列平衡2NO2
N2O4 (正反应放热)。当向A中加入10g NaOH固体使其溶解,往B中加入50g硝酸铵也使其溶解(20℃时,硝酸铵的溶解度为197g),则:
(1)A、B烧杯中,A杯溶液温度 ,
B杯溶液温度 (填升高、降低、不变)
(2)试管C中气体颜色变 ,D中气体颜色
变 ;(填“深”、“浅”、“不变”)
(3)在测定NO2相对分子质量时,下列条件较为适宜
的是
A.温度25℃,压强1.01×105Pa B.温度0℃,压强5.05×104Pa
C.温度130℃,压强5.05×103Pa D.温度130℃,压强3.03×105Pa
20、(12分)某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定烧碱的纯度,进行以下滴定操作:
①用碱式滴定管移取25 mL烧碱溶液于锥形瓶中,并滴加几滴酚酞试剂;
②在250 mL的容量瓶中定容成250 mL烧碱溶液;
③在天平上准确称取烧碱样品 w g,在烧杯中加蒸馏水溶解;
④将物质的量浓度为c mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数为v1 mL;
⑤在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积v2 mL。
回答下列问题:
(1)正确的操作步骤的顺序是(用①、②、③、④、⑤表示) ;
(2)滴定操作时眼睛应注视 ;
(3)若酸式滴定管没有用标准H2SO4润洗对测定结果有何影响?
(填“偏高”、“偏低”、或“无影响”,下同),若锥形瓶在滴定前预先用水润洗后未干燥,则滴定结果 。
(4)若在配制250 mL烧碱溶液时,不慎多加了一些水,超过瓶颈的刻度线,如何补救?
;
(5)该烧碱样品的纯度的计算式为 。
19、(8分)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,某学生设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
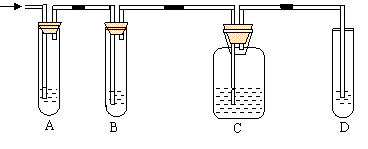
(1)实验室制乙烯反应方程式为:
(2)图中A、B、C、D装置可盛放的试剂是:①品红溶液 ②浓H2SO4 ③NaOH溶液④酸性KMnO4溶液,填写有关试剂的序号:
A 、B 、C 、D
(3)证明混合气体中的确含有乙烯的现象是
。
|
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
|
|
|
|
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
|
|
|
|
|
|
|
|
18、下列各组化合物中,不论二者以什么比例混合,只要总质量一定,则完全燃烧时生成水的质量不变的是 ( )
A.CH4、C2H6 B.C2H4、C3H6 C.C3H6、C6H6 D.C2H2、C6H6
第Ⅱ卷
17、甲苯苯环上的一个氢原子被烃基-C3H7所取代,可能得到的一元取代物有 ( )
A.3种 B.4种 C.6种 D.8种
16、向一定量的Fe、FeO、Fe2O3的混合物中加入100 mL 1.0 mol/L的盐酸,恰好使混合物完全溶解,放出224 mL的气体(标准状况)。所得溶液中加KSCN溶液后无红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是 ( )
A.2.8g B.5.6g C.8.4g D.11.2g
15、甲、乙两烧杯中各盛有100 mL 3 mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=1:2,则加入的铝粉质量为 ( )
A.1.8g B.3.6g C.5.4g D.7.2g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com