
题目列表(包括答案和解析)
5. 木炭屑与浓HNO3共热,产生的气体等分为①和②两份,将第一份气体先导入适量蒸馏水中再导入石灰水中,将第二份气体直接导入石灰水中,则石灰水的变化可能是
A、①不变浑浊,②变乳白色 B、①变乳白色,②不变浑浊
C、①变乳白色,②变乳白色 D、①不变浑浊,②变淡黄色
4. 关于白磷和红磷的下列说法中,不正确的是
A、白磷和红磷在一定条件下可以相互转化 B、燃烧产物均相同
C、都溶于二硫化碳 D、保存方法不同
3. 1L0.1mol·L-1氨水中所含溶质微粒的物质的量是
A、0.1molNH3分子
B、0.1molNH3·H2O分子
C、NH3分子和NH3·H2O分子约共0.1mol
D、NH3分子、NH3·H2O分子、 离子共0.1mol
离子共0.1mol
2. 在NO2被水吸收的反应中,发生还原反应和氧化反应的物质的量之比为
A、1:2 B、2:1 C、1:3 D、3:1
1. 下列关系不正确的是
A、非金属性:N>P>As>Sb>Bi
B、 酸性:HNO3>H3PO4>H3AsO4>H3SbO4>H3BiO4
C、 稳定性:NH3<PH3<AsH3<SbH3<BiH3
D、稳定性:HCl>H2S>PH3>SiH4
24.(本题满分8分)
二氧化氮在加热条件下能够分解成一氧化氮和氧气。
该反应进行到45秒时,达到平衡(N02浓度约为0.0125mol/L。右图中的曲线表示二氧化氮分解反应在前25秒内的反
应进程。
(1)请计算前20秒内氧气的平均生成速度:
(2)若反应延续至70秒,请在图中用实线画出25秒至70秒的反应进程曲线。
(3)若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出催化剂后的反应进程曲线。
(4)写出该反应的化学平衡常数表达式:
23.(本题满7分)
把9g铝镁合金投入40mL NaOH溶液中,测得反应产生的气体的体积为3.36L(标准况),加入足量盐酸后,残存的金属全部溶解,测得反应又产生6.72气体(标准状况)。试求:
(1)合金中镁的质量分数;
(2)原氢氧化钠溶液的物质的量浓度。
22.(10分)(1)0.02mol/L的HCN溶液与0.02mol/LNaCN溶液等体积混合,已知该混合溶液中
c(Na+)>c(CN-),用“>、<、=”符号填空
①溶液中,c(OH-) c(H+) ②c(HCN) c(CN-)
③c(HCN)+c(CN-) 0.02mol/L
(2)①向明矾溶液中逐滴滴人氢氧化钡溶液至硫酸根离子刚好沉淀完全时,溶液的pH
7(填>,、<、==,离子反应总方程式为 ;
②向明矾溶液中逐滴加氢氧化钠溶液至铝离子刚好沉淀完全时,溶液的PH
7(填>、<、=),离子反应总方程式为 。
21.(10分)高炉炼铁中发生的基本反应之一为:FeO(固)+CO(气)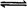 Fe(固)+CO2(气)(正反
Fe(固)+CO2(气)(正反
应为吸热反应),一定温度下,反应达到平衡时 的值为一常数.用K表示。已知 1100℃时K=0.263。
的值为一常数.用K表示。已知 1100℃时K=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO浓度的比值 。
平衡常数K值 。(本小题空格均备选:增大、减小或不变)
(2)1100°C时测得高炉中c(C02)=0.025mol/L,c(CO)=0.1 mol/L,在这种情况下,该反应
是否处于平衡状态 (填是或否),此时反应速率V正 V逆(填大于、
小于或等于)其原因是 。
20.(10分)有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿PH试纸,然后用洁
净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是 (填“正确的”或“错误的”),其理由是
。
(2)如不正确,请分析是否一定有误差? 。
(3)若用此法分析测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是
,原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com