
题目列表(包括答案和解析)
2.将锌片跟醋酸溶液反应,若在溶液中加入固体醋酸钠,则生成氢气的速率会( )
A.增大 B.减小 C.不变 D.先增大后减小
1.下列物质容易导电的是( )
A.熔融的氯化钠 B.无水酒精 C.硫酸铜晶体 D.硝酸钾溶液
26.(8分)合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1m3(标准状况)CH4按上式完全反应,产生H2 mol。
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1m3(标准状况)CH4按上述两式完全反应,产物气体的体积V(标准状况)为 。
(3)CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气氧气含量不同)混合反应,产物气体组成如下表:
|
气体 |
CO |
H2 |
N2 |
O2 |
|
体积(L) |
25 |
60 |
15 |
2.5 |
计算该富氧空气中O2和N2的体积比V(O2)/V(N2)。
(4)若CH4和H2O(g)及富氧空气混合反应的产物中,V(H2)/V(N2)=3︰1 (合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为何值?
25.(6分)3.2g Cu与过量硝酸 (a mol•L-1,20 mL )充分反应。硝酸的还原产物只有NO2、NO,反应后含H+为0.1 mol
(1)此时溶液中所含NO3-为________ mol
(2)求生成 的气体中NO2和NO的物质的量(用含a的式子表示)
24.(5分)用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可
选择使用,N2和O2的用量可自由控制)。
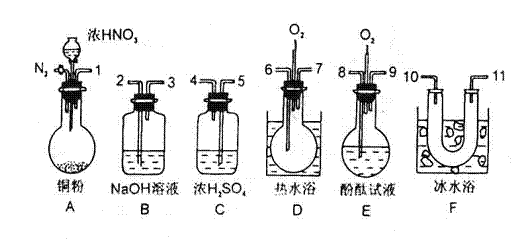
已知:①NO+NO2+2OH-→2NO2-+H2O②气体液化温度:NO2 21℃ NO -152℃
试回答:
(1)反应前先通入N2目的是
(2)确认气体中含NO的现象是
(3)装置F的作用是
(4)如果O2过量,则装置B中发生反应的化学方程式为:
22.(10分)Ⅰ 恒温、恒压下,在一个可变容积的容器中发生如下反应:(2003年江苏化学高考题)
A(气) + B(气) 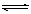 C(气)
C(气)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时A的物质的量
______mol
(2)若开始时放入3molA和3molB,达到平衡后,生成C的物质的量______mol
(3)若开始时放x molA.2 mol B和1 mol C,到过平衡后,A和C的物质的量分别是
y mol和3a mol ,则x = ______ mol, y = ________ mol
平衡时,B的物质的量__________ (选填一个编号)
(甲)大于2 mol (乙)等于2 mol
(丙)小于2 mol (丁)可能大于、等于或小于2 mol
作出此类判断的理由是___________________________________________
(4)若在(3)的平衡混合物中再加入3 mol C,待再次到达平衡后,C的物质的量分数是____
Ⅱ 若维持温度不变,在一个与⑴反应前起始体积相同,且容积固定的容器中发生上述反应
(5)开始时放入1 mol A和1 mol B到达平衡后生成b mol C。将b与⑴小题中的a进行比________(选填一个编号)
(甲)a < b (乙) a > b (丙) a = b (丁)不能比较两者大小
作此判断的理由__________________________________________
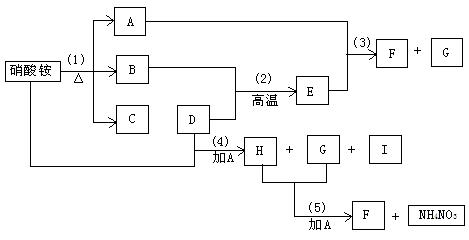 23.(5分)如图表示
23.(5分)如图表示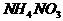 和D物质为起始反应物发生的一系列变化,其中在常温下A 为液体,F为不溶于水和碱溶液的白色固体,B.G、I为无色气体,其中G能使湿润的红色石蕊试纸变蓝。
和D物质为起始反应物发生的一系列变化,其中在常温下A 为液体,F为不溶于水和碱溶液的白色固体,B.G、I为无色气体,其中G能使湿润的红色石蕊试纸变蓝。
请填写以下空白:
(1)D是_______,E是______,H是________。
(2)反应(4)和(5)的离子方程式是_____________________。
21.(7分)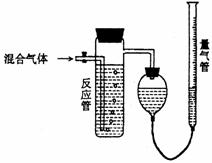 工业上测量SO2、N2、O2混合气体中
工业上测量SO2、N2、O2混合气体中
SO2含量的装置如下图;反应管中装有碘的淀
粉溶液。SO2和I2发生的反应为(N2、O2不与
I2反应):SO2+I2+2H2O→H2SO4+2HI
(1)混合气体进入反应管后,量气管内增加的
水的体积等于 的体积(填写气体的
分子式)。
(2)反应管内溶液蓝色消失卮,没有及时停止通气,则测得的SO2含量 (选填:
偏高,偏低,不受影响)。
(3)反应管内的碘的淀粉溶液也可以用 代替(填写物质名称)。
(4若碘溶液体积为VamL.,浓度为Cmol·L-1,N2与O2的体积为VbmL(已折算为标
准状况下的体积)。用C.VA.Vb表示SO2的体积百分含量为: 。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为. (选
下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
20.(6分)有NO2和N2O4常温常压下A.B.C.D均为气态。A与B可发生可逆反应:
A +
B 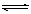 C +nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在
C +nD。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在
不同条件下达到平衡时C的浓度如下
|
温度 |
压强(kPa) |
C平衡浓度mol•L-1 |
|
25℃ |
100 |
1.0 |
|
25℃ |
200 |
1.8 |
|
25℃ |
300 |
3.2 |
|
25℃ |
400 |
6.0 |
(1)可逆反应中系数n的取值范围为______________理由 ________________________
(2)在500kPa时,D的状态可能为__________________________
19.(7分)(1)磷在自然界里主要以 的形式存在于矿石中。磷的单质有多种同
素异形体,其中最常见的是有毒的 和无毒的 。
(2)磷在不充足的氯气中燃烧的化学方程式为:
______________________________________
而在过量的氯气中燃烧的化学方程式则是:
___________________________________________
(3)磷(原子量为31)在空气中燃烧生成的氧化物通常可用作强干燥剂。制备100g
这种干燥剂所消耗的空气的体积约为 L(在标准状况下)。
18.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域
作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引
起整个化学领域正在经历一场革命性的变化。下列说法正确的是 ( )
A.化学不再是纯实验科学 B.化学不再需要实验
C.化学不做实验,就什么都不知道 D.未来化学的方向还是经验化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com