
题目列表(包括答案和解析)
8.稀H2SO4中插入一块铜片,加入下列物质后,可使Cu片迅速发生腐蚀的是( )
A.稀盐酸 B.FeCl3晶体 C.Na2SO4晶体 D.KNO3晶体
7.(2002年湖北八市联考)在密闭容器中一定量混合气体发生反应:2A(g)+B(g) xc(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
xc(g),达到平衡时测得A的浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大2倍,再达平衡时,测得A的浓度为0.3mol/L,下列有关判断正确的是( )
A.x=3 B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数增大
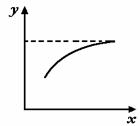
6.在密封容器中通入A、B两种气体,在一定条件下反应:2A(气)+B(气)  2c(气)+Q(Q>O)达到平衡后,改变一个条件(x),下列量(y)一定符合下图中曲线的是( )
2c(气)+Q(Q>O)达到平衡后,改变一个条件(x),下列量(y)一定符合下图中曲线的是( )
|
|
x |
y |
|
A |
再加入A |
B的转化率 |
|
B |
再加入C |
A的体积分数 |
|
C |
压强 |
A的转化率 |
|
D |
温度 |
混合气体的平均摩尔质量 |
5.在一个固定体积的密闭容器中,温度一定,发生反应:
H2(g)+Br2(g)  2HBr(g)
2HBr(g)
已知加入1molH2和2molBr2时,达到平衡后,生成amolHBr,在相同条件下,起始时加入H2、Br2、HBr的物质的量分别为x、y、z(均不为零),如果仍保持平衡时,各组分的组成不变,以下推断不正确的是( )
A.x、y应满足的关系是 y=2x
B.x、y、z应满足的关系是 4x+z=2y
C.达平衡时HBr的物质的量为 (x+y+z)·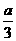 mol
mol
D.达平衡时HBr的物质的量一定仍为 amol
4.下列说法中,可以说明反应N2+3H2 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
A.1个N≡N键断裂的同时,有3个H-H键形成
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有6个N-H键断裂
D.1个N≡N键断裂的同时,有6个N-H键形成
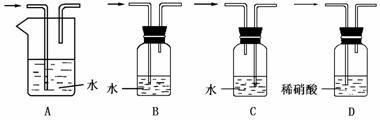
3.能除去NO中的NO2的试剂与装置是( )
2.反应速率v和反应物浓度的关系是用实验方法测定的.化学反应H2+Cl2 2HCl的反应速率v可表示v=K(c(H2))m·(c(Cl2))n,式中K为常数,m,n值可用下表中数据确定.由此可推得,m,n值正确的是( )
2HCl的反应速率v可表示v=K(c(H2))m·(c(Cl2))n,式中K为常数,m,n值可用下表中数据确定.由此可推得,m,n值正确的是( )
|
c(H2)(mol/L) |
c(Cl2)(mol/L) |
v(mol/(L·s)) |
|
1.0 |
1.0 |
1.0K |
|
2.0 |
1.0 |
2.0K |
|
2.0 |
4.0 |
4.0K |
A.m=1,n=1 B.m=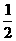 ,n=
,n=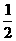 C.m=
C.m=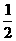 ,n=1 D.m=1,n=
,n=1 D.m=1,n=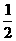
1.把下列4种X的溶液:①10mL2mol/L;②20mL2mol/L;③10mL4mol/L;④20mL3mol/L,分别加进4个盛有10mL2mol/L的盐酸的烧杯中,并均加水稀释至50mL,此时X和盐酸和缓地进行反应,则各烧杯中反应速率大小关系正确的是( )
A.①<②<③<④ B.①<②=③<④
C.①=②<④<③ D.①=③<②=④
25.由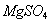 、
、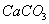 、
、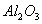 组成的混合粉末,其质量为44.2g,将其均匀地分为两份.若向其中的一份粉末中加入过量的盐酸,充分反应后,最多可收集到1.12L标准状况下的气体;若向另一份粉末中加入
组成的混合粉末,其质量为44.2g,将其均匀地分为两份.若向其中的一份粉末中加入过量的盐酸,充分反应后,最多可收集到1.12L标准状况下的气体;若向另一份粉末中加入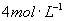 的氢氧化钠溶液100mL后,充分搅拌,有沉淀生成,若向此浊液中滴加
的氢氧化钠溶液100mL后,充分搅拌,有沉淀生成,若向此浊液中滴加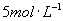 盐酸20mL沉淀没有减少,继续滴加盐酸则沉淀逐渐增加,当共加入
盐酸20mL沉淀没有减少,继续滴加盐酸则沉淀逐渐增加,当共加入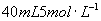 的盐酸时沉淀量达到最大值,请计算三种物质各自的质量分数.[已知碳酸的酸性强于
的盐酸时沉淀量达到最大值,请计算三种物质各自的质量分数.[已知碳酸的酸性强于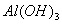 ]
]
24.5.8g丁烷完全燃烧后的产物全部通入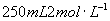 的氢氧化钠溶液中(设产物完全被吸收),试确定溶液中各溶质的物质的量浓度(设反应前后溶液体积不变)
的氢氧化钠溶液中(设产物完全被吸收),试确定溶液中各溶质的物质的量浓度(设反应前后溶液体积不变)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com