
题目列表(包括答案和解析)
25、(8分)有机物A、B分子式不同,它们只可能含碳、氢、氧元素中的两种或三种。如果将A、B不论以何种比例混合,只要其物质的量之和不变,完全燃烧后生成的CO2和消耗的氧气的物质的量也不变。那么:
(1)A、B满足的条件是
(2)试写出符合上述条件且分子量最小的A和B的结构简式
(3)若A为C3H4,则B可能的分子式为
(4)若A为C4H8O,则B的分子式可能是
24、(12分)有A、B、C、D、E、F6种有机物,它们是烃或烃的衍生物,在一定条件下,有下图所示转化关系
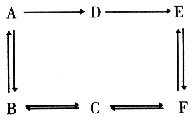
A可氧化成D,A的气体与相同条件下一氧化碳的密度相同,B与碱溶液共煮可得物质C和无机盐G,在反应后溶液中加入稀硝酸至酸性,再加硝酸银溶液得到淡黄色沉淀。
回答下列问题:
(1)B→A的反应属 反应,C和E→F的反应属 反应。
(2)按要求写出反应方程式(有机物用结构简式)
①B→A的反应方程式
②B→C的反应方程式
③D→E的离子方程式
④C和E→F的反应方程式
23、(12分)按下列要求写出有机物的分子式或结构式:
(1)与CH4含碳质量分数相同的两种有机物的分子式 , 。
(2)某有机物的分子式为C2H5O2N,写出可能的结构式:
, , , 。
22、(8分)1100℃时,在恒容闭容器中发生可逆反应:Na2SO4(s)+4H2(g) Na2S(s)+4H2O(g)△H=QKJ/mol,并达到平衡,回答以下问题:
Na2S(s)+4H2O(g)△H=QKJ/mol,并达到平衡,回答以下问题:
(1)降低温度平衡 移动(“正向”“逆向”“不发生”)
(2)加入少量Na2SO4,则平衡 移动(“正向”“逆向”“不发生”)
(3)加入少量灼热的Fe3O4粉末,则平衡 移动(“正向”“逆向”“不发生”)
(4)若初始时加入的Na2SO4是2.84g是2.8g,Na2SO4的平衡转化率为45%,则达到平衡时该容器内固体的总质量为 。
21、(8分)从H+、Na+、Cu2+、CI-、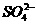 五种离子中恰当地组成电解质,按下列要求进行电解:
五种离子中恰当地组成电解质,按下列要求进行电解:
(1)以碳棒为电极,使电解质质量减少,水量不变进行电解,则采用的电解质是
(2)以铂片为电极,使电解质质量不变,水量减少进行电解,则可采用的电解质是
。
(3)以碳棒为阳极,铁棒为阴极,使电解质和水量都减少,则可采用的电解质是
(4)以铜棒为阳极,铁棒为阴极,使电解质和水量都不变,则可采用的电解质是
20、(12分)某液态卤代烷RX的密度是ag·cm-3,该RX可以跟稀碱发生水解反应,生成ROH(能跟水互溶)和HX,为了测定RX的分子量,拟定的实验步骤如下:
①准确量取该卤代烷bmL,放入锥形瓶中;
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热发生反应;
③反应完成后,冷却溶液,加稀HNO3酸化,滴加过量AgNO3溶液得到白色沉淀;
④过滤、洗涤、干燥后称重,得到固体cg
回答下面问题;
(1)装置中工玻璃管的作用是
(2)步骤④中洗涤的目的是为了除去沉淀上吸附的 离子;
(3)该卤代烷中所含卤素的名称是 ,判断的依据是 ;
(4)该卤代烷的相对分子质量是 (列出算式);
(5)如果在步骤③中,加HNO3的量不足,没有将溶液酸化,则步骤④中测得的C值(填下列选项代码) 。
A、偏大 B、偏小 C、不变 D、大小不定
19、(7分)向淀粉溶液中加入少量稀硫酸,并加热使之发生水解,请你设计实验,测定水解的程度:
(1)所用试剂
(2)操作现象结论
。
18、常温常压下,下列气态烃与O2的混合气体8L,充分反应后,将生成物通过浓H2SO4,恢复到原来状态,气体体积变为4L,则该烃可能是①CH4 ②C3H6 ③C3H8 ④C2H2
A、③⑤除外 B、⑤除外 C、仅①② D、①③④
第II卷
17、甲醛与某单烯烃的混合物含氧质量分数为x,则含碳、氢的质量分数为
A、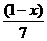 B、
B、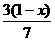 C、
C、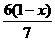 D、无法确定
D、无法确定
16、某有机物X能发生水解反应,水解产物为Y和Z,同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是
A、乙酸丙酯 B、甲酸乙酯 C、乙酸甲酯 D、乙酸乙酯
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com