
题目列表(包括答案和解析)
14、两种金属组成的合金25g与Cl2完全反应后,消耗Cl2 35.5g,则合金的可能组成是:
( )
A、钙和铜 B、铁和铝 C、钠和镁 D、铜和锌
13、将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是: ( )
A、CO2 B、NO2 C、H2S D、NH3
11、在FeCl3和BaCl2的混合溶液中通入SO2气体,观察到有白色沉淀生成,此沉淀是: ( )
A、BaSO4 B、BaSO3 C、S D、FeS
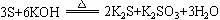
 12 、在
中,被还原的硫元素和被氧化的硫元素的质量比是: ( )
12 、在
中,被还原的硫元素和被氧化的硫元素的质量比是: ( )
A、3∶2 B、3∶1 C、2∶1 D、1∶1
9、Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4∶1,则溶液中NaCl与NaClO的物质的量之比为: ( )
A、11∶2 B、5∶1 C、1∶1 D、9∶4
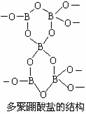 10、有一种多聚硼酸盐为无限空间网状结构,右图为其结构单元示意图。其结构的基本单元可表示为(B5On)m-,则m、n的值分别为
10、有一种多聚硼酸盐为无限空间网状结构,右图为其结构单元示意图。其结构的基本单元可表示为(B5On)m-,则m、n的值分别为
( )
A、3,9 B、2,4
C、2,5 D、3,6
8、将0.1mol/L的K2SO4溶液、0.2mol/L的Al2(SO4)3溶液和蒸馏水混合,要使混合溶液中K+浓度为0.1 mol/L,Al3+浓度为0.1 mol/L,SO42-浓度为0.2mol/L,则所取K2SO4溶液、Al2(SO4)3溶液和蒸馏水三者的体积比是: ( )
A、2∶1∶2 B、1∶1∶2 C、2∶1∶1 D、1∶1∶1
7、现有一种含Ag+、Al3+、Mg2+、Ba2+的混合液,要使上述四种离子利用沉淀反应逐一分离出来,加入试剂(溶液)的顺序依次是: ( )
A、NaOH、NaCl、HCl、Na2SO4 B、HCl、NaOH、Na2SO4、NaCl
C、Na2SO4、NaOH、NaCl、HCl D、NaCl、Na2SO4、NaOH、HCl
6、下列各组中的离子,因发生氧化还原反应而不能大量共存的是: ( )
A、Fe3+ K+ OH- Cl- B、SO42- Fe2+ Cl- I-
C、S2- Cl- NO3- H+ D、Al3+ Ag+ Na+ Cl-
5、0.096kg碳完全燃烧生成二氧化碳气体放出3143.4kJ热量,以下热化学方程式的表示中正确的是: ( )
A、C(s) + O2(g) =CO2(g);ΔH = -392.9kJ/mol
B、C(s) + O2(g) =CO2(g);ΔH = -196.5kJ/mol
C、C(s) + O2(g) =CO2(g);ΔH = +392.9kJ/mol
D、C + O2 =CO2;ΔH = -392.9kJ/mol
4、下列各组物质的晶体中,化学键类型和晶体类型都相同的是: ( )
A、SO2和SiO2 B、NaCl和HCl C、CCl4和KCl D、CO2和H2O
3、将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是: ( )
A、NaOH浓溶液 B、NaCl浓溶液 C、沸水 D、冷水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com