
题目列表(包括答案和解析)
3.下列物质属于纯净物的是( )
A.王水 B.硝铵 C.漂白粉 D.氨水
2. 在一定条件下,发生反应:2NO2 N2O4,该反应达到化学平衡后,降低温度,混合物的颜色变浅,下列有关说法正确的是( )
N2O4,该反应达到化学平衡后,降低温度,混合物的颜色变浅,下列有关说法正确的是( )
A.正反应为放热反应 B.正反应为吸热反应
C.降温后NO2的浓度增大 D.降温后各物质的浓度不变
1. 汽车尾气中污染空气的成分有( )
①CO2 ②CO ③NO ④铅的化合物
A.①②③ B.①③④ C.②③④ D.①②③④
26、Ⅰ、恒温、恒容下,在一个密闭的容器中发生如下反应:
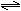 A(g)+ B(g) 2C(g)
A(g)+ B(g) 2C(g)
(1)若开始时放入1 mol A和1 mol B,到达平衡后,生成a mol C,这时A的物质的量为 mol;
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为 mol;此时C的质量分数与(1)比较 (填相等、大于或小于);
(3)若开始时,放入x mol A,2 mol B和2 mol c到达平衡后,A和C的物质的量分别是y mol和3a mol,则x = mol, y = mol;开始时的反应将向 (选填一个编号) 。
(甲)正向移动 (乙)逆向移动
(丙)可能正向,可能逆向移动 (丁)平衡不移动
作出此判断的理由是 。
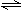 Ⅱ、若在相同条件下的反应为:A(g)+ B(s) 2C(g),开始时加入1 mol A、1 mol B,反应达平衡时生成C为0.2 mol,则按下列配比加入后,达平衡时生成C的物质的量仍为0.2 mol的是
Ⅱ、若在相同条件下的反应为:A(g)+ B(s) 2C(g),开始时加入1 mol A、1 mol B,反应达平衡时生成C为0.2 mol,则按下列配比加入后,达平衡时生成C的物质的量仍为0.2 mol的是
A. 2 mol C B. 1 mol A + 0.5 mol B
C. 0.5 mol A + 0.5 mol B + 1 mol C D. 2 mol A + 2 mol B
25、50mL0.1mol/LBaCl2与100mL0.75mol/L H2SO4溶液混合,求:
⑴产生沉淀多少克?
⑵反应后溶液的pH为多少?
24、有A、B、C、D、E五种化合物,其中A、B、C、D是含铝元素的化合物,F是一种气体,标准状态下对空气的相对密度为1.103。且有下列转化关系:
①A+NaOH→D+H2O;②B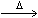 A+H2O;③C+NaOH(适量)→B+NaCl;
A+H2O;③C+NaOH(适量)→B+NaCl;
④E+H2O→NaOH+F;⑤C+D+H2O→B+……
回答下列问题:
(1)化学式:A__________,B__________,C__________,D__________。
(2)写出C溶液与D溶液反应的化学方程式:_____________________。
(3)写出4molC和6molE在水溶液中发生反应的化学方程式(写出一个总反应的化学方程式):____________________________________。
23、(1) 溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为有
溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为有 的水溶液中存在如下平衡:
的水溶液中存在如下平衡:
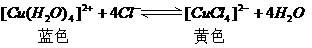
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法:①___________,
②_______________。
(2)在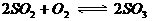 的平衡体系中,加入
的平衡体系中,加入 构成氧气,当平衡发生移动后,
构成氧气,当平衡发生移动后,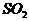 中
中 的含量_________(填增加、减少或不变),其原因是__________。
的含量_________(填增加、减少或不变),其原因是__________。
22.今有①CH3COOH、②HCl、③H2SO4 三种溶液,选择填空:
A.①>②>③ B.①<②<③ C.①=②=③ D.①=③>②
E.①>②=③ F.①<②=③ G.①=②<③ H.①=②>③
(1)当它们pH相同时,其物质的量浓度关系是 A 。
(2)当它们的物质的量浓度相同时,其pH的关系是A 。
(3)中和等体积、等物质的量浓度的烧碱溶液,需同物质的量浓度的三种酸溶液的体积关系为 H 。
(4)体积和物质的量浓度相同的①、②、③三溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为 B 。
(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为 E 。
(6)当它们pH相同、体积相同时,同时加入锌,则开始时反应速率 C ,若产生相同体积的气体(相同状况),所需时间 F 。
(7)将pH相同的三种酸均稀释10倍后,pH关系为 F 。
21、在一定温度下,把
2mol SO2和1mol O2通入一个容积固定的密闭容器里,发生如下反应: 。当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的质量分数仍跟上述平衡的完全相同。请填写下列空白:
。当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的质量分数仍跟上述平衡的完全相同。请填写下列空白:
(1)若a=0,b=0,则c=___________。
(2)若a=0.5,则b=___________,c=___________.
(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c)___________,___________。
20、某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A、在250mL的容量瓶中定容成250mL烧碱溶液
B、用移液管移取25mL烧碱溶液于锥形瓶中滴加几滴甲基橙指示剂
C、在天平上准确称取烧碱样品Wg,在烧杯中加蒸馏水溶解
D、将物质的量浓度为Mmol·L-1的标准的H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度数V1mL
E、在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度数为V2mL
回答下列问题:
(1)正确的操作步骤的顺序是(用字母填写):_____→_____→_____→_____→_____
(2)向滴定管中装入标准液后,液面应调整到的位置一般为:________________。
(3)操作E中在锥形瓶下垫一张白纸的作用是__________________。滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视___________。
(4)下列操作可能使测定结果偏低的是___________。
A、酸式滴定管在装液前未用标准H2SO4溶液润洗2次-3次
B、开始实验时,酸式滴定管尖嘴部分有气泡,在滴定过程中,气泡消失
C、滴定过程中,锥形瓶内溶液颜色变化由黄色变橙色,但立即又变为黄色,此时即记下滴定管液面所示的刻度
D、达到滴定终点时,俯视溶液凹面最低点读数(滴定前读数准确)
E、盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗
(5)如果所用酸式滴定管为50mL滴定管,实验完毕后,酸式滴定管中所剩标准液体积为___________。
A、V2mL B、(50-V2)mL
C、大于(50-V2)mL D、小于(50-V2)mL
(6)该烧碱样品中的纯度计算为______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com