
题目列表(包括答案和解析)
8.某地有甲、乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、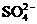 、
、 、OH-.若两厂单独排放都会造成严重的水污染.如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清,只含硝酸钠而排放,污染程度会大大降低.关于污染的分析,你认为正确的是( )
、OH-.若两厂单独排放都会造成严重的水污染.如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清,只含硝酸钠而排放,污染程度会大大降低.关于污染的分析,你认为正确的是( )
A. 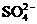 和
和 可能来自同一工厂
可能来自同一工厂
B.Cl-和 一定在不同工厂
一定在不同工厂
C.Ag+和Na+可能在同一工厂
D.Na+和 来自同一工厂
来自同一工厂
7.有五瓶溶液分别是①10ml0.60mol/LNaOH水碱 ②20ml0.05mol/LH2SO4水溶液 ③30ml0.04mol/L HCl水溶液 ④40ml0.30mol/L 水溶液 ⑤50ml0.02mol/L 蔗糖水溶液.以上各瓶溶液所含离子、分子总数的大小顺序是( )
A.①>②>③>④>⑤ B.②>①>③>④>⑤
C.②>③>④>①>⑤ D.⑤>④>③>②>①
6.将K2SO4、KAl(SO4)2、Al2(SO4)3三种盐混合于硫酸酸化物的水中,测得c(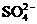 )=0.105mol/L
c(Al3+)=0.005mol/L,溶液的PH=2.0(假设溶液中H2SO4完全电离为H+和
)=0.105mol/L
c(Al3+)=0.005mol/L,溶液的PH=2.0(假设溶液中H2SO4完全电离为H+和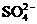 ,则c(K+)为( )
,则c(K+)为( )
A.0.045mol/L B.0.035mol/L
C.0.005mol/L D.0.040mol/L
5.PH和体积都相同的醋酸和硫酸溶液,将它们分别跟足量的碳酸钠溶液反应,在相同条件下,放出CO2气体的体积( )
A.一样多 B.醋酸比硫酸多
C.硫酸比醋酸多 D.无法比较
4.实验室中,某学生先用蒸馏水润湿PH试纸(每次使用时润湿程度相同),然后用洁净干燥的玻璃棒蘸取试液进行测定试液的PH,下列说法正确的是( )
A.该生的测定一定有误差产生
B.当溶液为中性时,该生的测定值不会有误差
C.用此方法检测c(H+)相等的盐酸和醋酸两溶液时,盐酸的PH比醋酸小
D.用此方法检测c(H+)相等的盐酸和醋酸两溶液时醋酸的PH比盐酸小
3.已知100℃时,水的离子积常数为1×10-12.在此温度下,将PH=8的NaOH溶液与PH=4的H2SO4溶液混合,得到PH=7的混合溶液,则NaOH溶液与H2SO4溶液的体积比约为( )
A.9∶11 B.9∶1 C.1∶9 D.11∶9
2.酸雨是过度燃烧煤和石油,生成硫、氮的氧化物,溶于水生成硫酸和硝酸的缘故,某次雨水分析数据如下:c(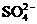 )=2.6×10-5mol/L,c(Cl-)=8.0×10-6mol/L,c(NH+4)=3.0×10-6mol/L,c(Na+)=1.0×10-6mol/L,c(NO-3)=2.4×10-5mol/L,则此次酸雨的PH接近于(lg8=0.9)( )
)=2.6×10-5mol/L,c(Cl-)=8.0×10-6mol/L,c(NH+4)=3.0×10-6mol/L,c(Na+)=1.0×10-6mol/L,c(NO-3)=2.4×10-5mol/L,则此次酸雨的PH接近于(lg8=0.9)( )
A.6.5 B.5 C.4 D.4.5
1.下列四种溶液中,由水电离生成的氢离子浓度之比①∶②∶③∶④是( )
①PH=0的盐酸 ②0.1mol/L的盐酸 ③0.01mol/L的NaOH溶液 ④PH=11的NaOH溶液
A.1∶10∶100∶1000 B.0∶1∶12∶11
C.14∶13∶12∶11 D.14∶13∶2∶3
35.氢氧化镁难溶于水,但它所溶解的那一部分则在溶液中完全电离,t℃时,饱和氢氧化镁溶液的PH=11,若不考虑KW值的变化,则该温度下氢氧化镁的溶解度是多少?(设溶液的密度等于1.0g/cm3)
[素质优化训练]
34.某工厂排放出的废水,经测定含有0.001mol/L的游离氯(Cl2)和0.008mol/L的H+,现采用Na2SO3除去其中的游离氯,有关反应如下:
Na2SO3+Cl2+H2O=Na2SO4+2HCl
若要处理5L这样的废水.
(1)需加入0.5mol/LNa2SO3溶液多少ml,才能将Cl2全部除去?
(2)处理后的废水的PH是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com