
题目列表(包括答案和解析)
2.( )下列单质中,通常用于制造半导体材料的是:A.金刚石;B.晶体硅;C.铁;D.铝。
1.( )下列变化属于物理变化的是:A.石油分馏;B.煤的干馏;C.油脂硬化;D.石油裂化。
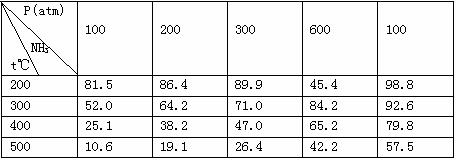
5.合成氨工业用氢气和氮气在催化剂作用下直接合成,右表表示在一定温度和压强下达到动态平衡时氨的体积分数.
其中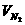 ∶
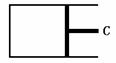
∶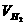 =1∶3.如图所示装置是一透热性很好的坚固容器,活塞C可左右移动,其总体积为44.8L,现将400℃、300大气压的H233.6L和400℃,300大气压的N211.2L充入容器中,当两者反应达到动态平衡时,若保持混合气体的压强仍为400℃、300大气压,求:
=1∶3.如图所示装置是一透热性很好的坚固容器,活塞C可左右移动,其总体积为44.8L,现将400℃、300大气压的H233.6L和400℃,300大气压的N211.2L充入容器中,当两者反应达到动态平衡时,若保持混合气体的压强仍为400℃、300大气压,求:
(1)容器是向外界放热,还是吸热?
(2)充入的N2的物质的量是多少?充入的H2转化率是多少?
(3)活塞C要向左侧移动的距离与容器全长之比是多大?
4.某农科所研究人员把棚内空气中的CO2浓度提高3-5倍,并将O2浓度尽量减少,结果取得良好的增产效果.从反应:

得到的启发是: .
3.在上题的系统里,同时发生反应:
SO2(g)+ 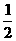 O2(g)
O2(g)  SO3(g)
SO3(g)
K=20,经测定,汽车的尾气原有SO2气体的浓度为2×10-4mol·L-1.问SO3的平衡浓度?
2.反应CO(g)+ 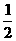 O2(g)
O2(g)  CO2(g)在1600℃时,K=1×104.经测定汽车尾气里的CO和CO2的浓度分别为4.0×10-5mol·L-1和4.0×10-4mol·L-1.若在汽车的排气管上增加一个1600℃的补燃器,并使其中的O2浓度始终保持4.0×10-4mol·L-1,求CO的平衡浓度和补燃器转化率.
CO2(g)在1600℃时,K=1×104.经测定汽车尾气里的CO和CO2的浓度分别为4.0×10-5mol·L-1和4.0×10-4mol·L-1.若在汽车的排气管上增加一个1600℃的补燃器,并使其中的O2浓度始终保持4.0×10-4mol·L-1,求CO的平衡浓度和补燃器转化率.
1.有文献报导:硫在空气中燃烧时,产物中的SO3约占5%-6%(体积),而硫在纯氧中燃烧时,其产物中的SO3约占2%-3%(体积),你能解释这一现象吗?试试看!
(提示:S+O2 SO2放出热量如何影响化学平衡2SO2(g)+O2(g)
SO2放出热量如何影响化学平衡2SO2(g)+O2(g)  2SO3(g)+Q)
2SO3(g)+Q)
8.有些反应从表面上看不能进行.如:
(1)KClO4+H2SO4 HClO4+KHSO4 (2)Na+KCl
HClO4+KHSO4 (2)Na+KCl NaCl+K
NaCl+K
(3)Mg+RbCl MgCl2+Rb (4)KCl+NaNO3
MgCl2+Rb (4)KCl+NaNO3 NaCl+KNO3
NaCl+KNO3
而实际生产中恰被用来制取带横线的物质.这4个反应中利用的反应原理相同的是 ,其原理是 ,不相同的原理是 .
[生活实际运用]
7.以H2、CO为主要组成,供化学合成用的一种原料气叫做“合成气”.若用天然气为原料制合成气,可用“天然气蒸气转化”的反应:
CH4(g)+H2O(g)  CO(g)+3H2(g)-Q
CO(g)+3H2(g)-Q
生产时主要条件是温度、压强和水蒸气的配比,另外还要有适宜的催化剂.合成气里的H2可用于合成氨,CO最终分离出来后可用于合成甲醇、醋酸、乙二醇等,即新兴起的以分子中只含有一个碳原子的化合物为原料来合成化工产品的“C1化学”.据此回答以下两题:
(1)天然气蒸气转化的主要反应进行时,有关叙述中不正确的是( )
A.反应速率为3v(H2)=v(CH4)
B.温度为800℃-820℃,若超过1500℃反而不利
C.工业上为使平衡正向移动,要用过量的天然气
D.在加压的条件下,正反应速率会增大
(2)目前用合成气生成甲醇时,采用Zn-Cr催化剂,其反应为:
CO(g)+2H2(g)  CH3OH(g)+Q
CH3OH(g)+Q
有关叙述正确的是( )
A.达到平衡时,容器内的总压保持不变
B.合成甲醇的反应可以认为是CO的氧化反应
C.根据勒夏特列原理,合成甲醇的反应要在加压和维持相当高的温度下进行,以利于提高单位时间内的产量
D.甲醇与CO能在一定条件下化合生成醋酸是因CO插入CH3OH中形成C=O键而成
6.合成氨厂常通过测定反应前后混合气体的密度来确定氮气的转化率.某工厂测得合成塔中N2、H2混合气体的密度为0.5536g/L(标况下测定),从合成塔出来的混合气体在相同条件下密度为0.693g/L.求该合成氨厂N2的转化率.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com