
题目列表(包括答案和解析)
1、下列无色气体中,遇空气变成红棕色的是( ) A.CO B.HCl C.SO2 D.NO
21、2个氢键,所以键能为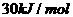
20、(1)N2H62++2OH-=N2H4+2H2O
(2)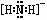
(3)22
(4)N2O CO2 CNO- BeF2 CaH2 等
(5)直线型(1分)
(6)一个单位正电荷
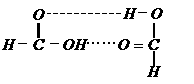
19、棕色、紫色,因为温度升高,分子间作用力减弱。
18、(1)b (2)H (3)①1S22S22P63S23P1 ② 镁 b、c
17、用VSEPR 理论判断:
|
物质 |
孤对电子对数 |
轨道杂化形式 |
分子或离子的形状 |
|
SO3 |
0 |
Sp2 |
平面三角形 |
|
PO43- |
0 |
Sp3 |
正四面体 |
|
NCl3 |
1 |
Sp3 |
三角锥形 |
21、二聚甲酸解聚反应为:(HCOOH)2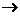 2HCOOH,该反应需吸收
2HCOOH,该反应需吸收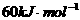 的能量,此能量是
断开
所需的能量,所以此键的键能为
的能量,此能量是
断开
所需的能量,所以此键的键能为 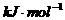 。写出(HCOOH)2的结构式
。
。写出(HCOOH)2的结构式
。
化学选修3 分子空间结构与物质性质测试题
20、氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)写出N2H62+与碱溶液反应的离子方程式 。
(2)NH2-的电子式为 。
(3)N3-有 个电子。
(4)写出N3-等电子体物质的化学式 。(一种)
(5)等电子数的微粒往往具有相似的结构,试预测N3-的构型 。
(6)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是
。
19、碘在不同溶剂中呈现紫色、棕色,一般认为溶液呈紫色时表明溶解了的“碘分子”并未和溶剂发生很强的结合。已知不同温度下,碘在石蜡油中的溶液呈紫色或棕色。请回答:温度低时溶液呈 色,温度高时溶液呈 色,因为
。
18、
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)在上面元素周期表中全部是金属元素的区域为 。
(a) A (b) B (c) C (d) D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是 。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①画出甲原子的基态电子排布:
甲 。
② 甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com