
题目列表(包括答案和解析)
5. 将过量的CO2分别通入①CaCl2溶液 ②Na2Si03溶液 ③Ca(CIO)2溶液 ④饱和
Na2CO3溶液。最终溶液中有白色沉淀析出的是
A.①②③④ B.②④ C.①②③ D.②③④
4. 在容积为672 mL的烧瓶里充满NO、NO2的混合气体,将其倒立在水槽里,去塞后再通人280 mL氧气,恰好完全反应,且水充满烧瓶(气体体积都折合成标准状况下)。下列有关叙述中,正确的是
A.总反应为NO+ NO2+O2+H2O=2HNO3
B.总反应为4NO+8 NO2+5O2+6H2O=12HNO3
C.生成HNO3的物质的量浓度接近O.03 mol·L-1
D.生成HNO3的物质的量浓度约为0.045 mol·L-1
3. 超临界液体是物质介于气态和液态之间的一种新的状态。目前应用最广的是超临界二氧
化碳,在化学工业中可取代氟利昂等溶剂、发泡剂。下列有关超临界二氧化碳的说法中错
误的是
A.超临界二氧化碳是新合成的一种物质
B.超临界二氧化碳由C02分子组成
C.用超临界二氧化碳溶解物质后,可在常温常压使二氧化碳挥发将其除去
D.用超临界二氧化碳代替氟利昂可减轻对臭氧层的破坏
2. 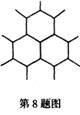 石墨是层状晶体,每一层内,碳原子排列成正六边形,许多个正六边形排列成平面网状结构。如果每两个相邻碳原子间可以形成一个碳碳单键,则石墨晶体中每一层碳原子数与碳碳单键数的比是
石墨是层状晶体,每一层内,碳原子排列成正六边形,许多个正六边形排列成平面网状结构。如果每两个相邻碳原子间可以形成一个碳碳单键,则石墨晶体中每一层碳原子数与碳碳单键数的比是
A.1:1 B.1:2 C.1:3 D.2:3
1. 将SO2气体通人BaCl2溶液至饱和,未见有沉淀生成,继续通入另一种气体仍无沉淀产
生。则通入的气体可能是
A.CO2 B.NH3 C.NO2 D.C12
19.量取25.00mL未知浓度的硝酸溶液,用去10.50mL浓度为0.120mol·L-1NaOH溶液进行滴定,又再用去14.50mL浓度为0.120mol·L-1的KOH继续滴定恰好安全反应,求该HNO3溶液的浓度是多少?
*20.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A 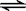 H++HA-,
H++HA-,
HA-
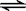 H++A2-,已知K1>K2,设有下列四种溶液:
H++A2-,已知K1>K2,设有下列四种溶液:
A.0.01 mol·L-1的H2A溶液
B.0.01 mol·L-1的NaHA溶液
C.0.02 mol·L-1的HCl溶液与0.04 mol·L-1的NaHA溶液等体积混合
D.0.02 mol·L-1的NaOH溶液与0.02 mol·L-1的NaHA溶液等体积混合
据此填写下列空白(填代号):
(1)c(H+)最大的是 ,最小的是 。
(2)c(H2A)最大的是 ,最小的是 。
(3)c(A2-)最大的是 ,最小的是 。
18.如图
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为4,量筒中液体体积是 mL。
(2)图II表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(50-a)mL
C.一定大于a mL D.一定大于(50-a)mL
17.(6分)某可溶性盐的化学式XmYn(m≠n),将一定量的该盐溶于适量的水中。
(1)若测得溶液的pH为3,则该盐与水反应的离子方程式可能为
。
(2)若该盐水溶液的pH为11,则其与水反应的离子方程式可能为
。
16.(10分)当滴有少量CH3COOH的CH3COONH4的混合物溶于水后,存在着的电离或离子反应的平衡有:
(1) ,(2) 。
(3) 。
由于 平衡的存在,抑制了 平衡的移动。
15.(16分)根据NH2·H2O的电离方程式 。结合变化量填下表。
|
H2O |
NH4Cl
(s) |
NaOH
(s) |
HCl
(1) |
||||||||||||||||||
|
(1)Kb |
|
|
|
|
||||||||||||||||||
|
(2)n
(OH-) |
|
|
|
|
||||||||||||||||||
|
(3)c (OH-) |
|
|
|
|
||||||||||||||||||
|
(4)平衡移动方向 |
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com