
题目列表(包括答案和解析)
12、下列反应达到平衡后,增大压强或升高温度,平衡都向正反应方向移动的是 ( )
A.2NO2(g) 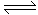 N2O4(g)(正反应为放热反应)
N2O4(g)(正反应为放热反应)
B.3O2(g) 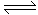 2O3(g)(正反应为吸热反应)
2O3(g)(正反应为吸热反应)
C.H2(g)+I2(g)
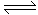 2HI(g)(正反应为放热反应)
2HI(g)(正反应为放热反应)
D.NH4HCO3(s) 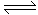 NH3(g)+H2O(g)+CO2(g)(正反应为吸热反应)
NH3(g)+H2O(g)+CO2(g)(正反应为吸热反应)
11.在一定条件下化学反应:2SO2(g)+O2(g) 2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个恒容容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
2SO3(g);△H=-197 kJ/mol 现有容积相同的甲、乙、丙三个恒容容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
|
容器 |
SO2(mol) |
O2(mol) |
N2(mol) |
Q(kJ) |
|
甲 |
2 |
1 |
0 |
Q1 |
|
乙 |
1 |
0.5 |
0 |
Q2 |
|
丙 |
1 |
0.5 |
1 |
Q3 |
根据以上数据,下列叙述不正确的是( )
A.在上述条件下反应生成1 molSO3气体放热98.5 kJ
B.丙容器中N2对反应热无影响。
C.Q1=2Q2=2Q3=197
D.2Q2=2Q3<Q1<197 kJ
10.常温下将稀NaOH溶液与稀醋酸溶液混合,不可能出现的结果是 ( )
A、pH>7, 且c(Na+)>c(OH-)> c(CH3COO-)> c(H+)
B、pH>7, 且c(Na+)+ c(H+)=c(OH-)+ c(CH3COO-)
C、pH<7, 且c(CH3COO-) > c(H+)> c(Na+)> c(OH-)
D、pH=7, 且c(CH3COO-)>c(Na+)>c(OH-)= c(H+)
9.下列反应离子方程式正确的是( )
A.溴化亚铁溶液中通入过量氯气:
Fe2+ + 2Br- + 2Cl2= Fe3+ + Br2 + 4Cl-
B.氯气通入冷的氢氧化钠溶液中: 2Cl2 + 2OH- = 3Cl-+ ClO-+ H2O
C.向澄清石灰水中加入少量小苏打溶液: Ca2+ + OH-+ HCO3- =CaCO3↓+ H2O
D.氨水中通入过量二氧化硫: 2NH3·H2O + SO2 = 2NH4+ + SO32-+ 2H2O
8.在铜的催化作用下氨气与氟气反应,得到一种三角锥形分子M和一种铵盐N。下列有关说法不正确的是 ( )
A.该反应的化学方程式为4NH3+3F2=NF3+3NH4F
B.M是极性分子,其还原性比NH3强
C.M既是氧化产物,又是还原产物
D.N中既含有离子键,又含有共价键
7.有人欲配制含下列不同阴、阳离子的溶液,其中能配制成功的是 ( )
A.Na+、NH4+、Cl-、NO3- B.Ba2+、NH4+、CO32-、HCO3-
C.H+、K+、I-、ClO- D.Cu2+、Na+、S2-、SO42-
6.下列各组物质混合后,既产生无色气体,又产生白色沉淀的是:
①Ba(NO3)2稀溶液跟NaHSO3溶液,②Ba(OH)2溶液跟(NH4)2SO4溶液共热,
③电石跟苏打水,④三氯化铁溶液跟碳酸氢钠溶液。( )
A.①②③④ B.②③ C.①②③ D.②③④
5、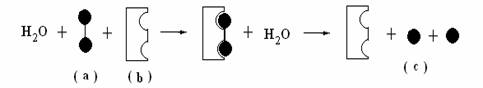 已知有一过程如下:
已知有一过程如下:
根据上图,a、b、c可分别表示( )
A、淀粉、酶、葡萄糖 B、蔗糖、酶、果糖
C、纤维素、酶、葡萄糖 D、麦芽糖、酶、葡萄糖
4..下列说法中正确的是(NA表示阿伏加德罗常数) ( )
A.273℃、1.01×105 Pa下,NA个H2分子所占体积约为22.4 L
B.2.3 g金属钠变成离子时失去的电子数目为NA
C.1 L 1 mol·L-1的CH3COOH溶液中,CH3COO-数目为NA
D.常温常压下,16 g臭氧所含的氧原子数目为NA
3.下列叙述中,正确的是 ( )
A.淀粉、纤维素互为同分异构体,都属于糖类;硝酸纤维、醋酸纤维都属于酯类
B.骨胶、皮胶以及日常生活中常用的糨糊、胶水都是黏合剂
C.相对分子质量相同、组成元素也相同,但分子结构不同、性质也不同的两种有机物一定是同分异构体
D.由一个有机物分子在一定条件下反应生成一个新的有机物分子和一个无机物分子的反应一定是消去反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com