
题目列表(包括答案和解析)
5.在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:
X(g)+2Y(g) 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
A 容器内密度不随时间变化
B 容器内各物质的浓度不随时间变化
C 容器内X、Y、Z的浓度之比为1︰2︰2
D 单位时间消耗0.1mol X同时生成0.2mol Z
4.下列事实不能说明亚硝酸(HNO2)是弱酸的是
A、HNO2不与NaCl反应
B、HNO2与同浓度的盐酸溶液作对比导电实验,灯泡很暗
C、室温下NaNO2溶液的pH值大于7
D、室温下0.1 mol /L HNO2溶液的pH = 2.1
3.对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是
A.加入适量的氯化铵晶体后,两溶液的pH均碱小
B.温度下降10ºC,两溶液的pH均不变
C.分别加水稀释10倍,两溶液的pH仍相等
D.用盐酸中和,消耗的盐酸体积相同
2.对于反应2A(g)+3B(g)=C(g)+5D(g),在某段时间内的平均反应速率为 ,(x代表某反应物或生成物)之间的关系,正确的是
,(x代表某反应物或生成物)之间的关系,正确的是
A. B.
B.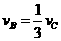 C.
C. D.
D.
1.下列三种化合物由左到右是按强电解质、弱电解质、非电解质的顺序排列的一组是
A、HCl、CaCO3、SO2 B、HClO、H2S、C2H5OH
C、KNO3、CH3COOH、NH3 D、BaSO4、H3PO4、H2O
22. (8分)将 等 物 质 的 量 的 A,B 混 合 于2 L 的 密 闭 容 器 中,发 生 反 应
3A(g)+ B(g) xC(g) + 2D(g)。经5min分钟后达到平衡时,测知D的浓
xC(g) + 2D(g)。经5min分钟后达到平衡时,测知D的浓
度为0.5mol/L,[ A] :[ B] = 3 :5,C的平均反应速率为0.1mol·(L·min)-1 试求
(1)A的平衡浓度是多少?(2)B的平均反应速率?(3)x = ?
20. (4分) 用 pH 试纸测定溶液的 pH 时,为什么不能先用蒸馏水润湿试纸 ?
答:
21(11分)实验室用氨气还原氧化铜方法测定铜的近似相对原子质量, 反应的化学方程式为:

 试回答:(1)如果选用测定反应物CuO和生成物H2O的质量(mCuo、
试回答:(1)如果选用测定反应物CuO和生成物H2O的质量(mCuo、
① (5分)仪器连接的顺序(用字母编号表示,仪器可重复使用) ;
d中浓硫酸的作用是 , ;
实验完毕时观察到a中的现象是 ;
② (2分)列出计算Cu的相对原子质量的表达式 ;
③ (2分)下列情况将使测定结果偏大的是 .
(以下选择填空不限1个正确答案,均用字母编号填写)
(a) CuO未全部还原为Cu (b)CuO受潮 (c)CuO中混有Cu
(2)(2分)如果仍采用上述仪器装置,其他方案可选用测定的物理量有


19. (9分)下图 分别代表有关反应中的一种物质,请填下以下空白。
分别代表有关反应中的一种物质,请填下以下空白。
(已知二氧化碳能与镁反应生成氧化镁和另一种单质)
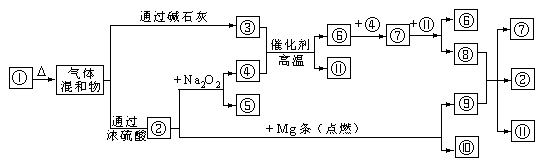
(1)(6分)①、③、④的化学式分别是 、 、 。 (2)(3分)⑧与⑨反应的化学方程式是 。
18. (10分)化学平衡移动原理,同样也适用于其它平衡,已知在氨水中存在下列平衡:
NH3 + H2O NH3·H2O
NH3·H2O NH4+ + OH-
NH4+ + OH-
(1)(3分)向氨水中加入CuSO4固体时平衡向 移动,OH-离子的浓度 ,
NH4+ 的浓度 。
(2)(4分)向氨水中加入浓盐酸,平衡向 移动,此时溶液中浓度减小的
粒子有 、 、 。
(3)(3分)向浓氨水中加入少量的NaOH 固体,平衡向 移动,此时发生的现
象是 。
17. (8分)对于mA(g)+nB(g)
(8分)对于mA(g)+nB(g) pC(g) + Q有如图所示的关系,
pC(g) + Q有如图所示的关系,
(图中C%为C的质量分数)则
(1)P1与P2 的关系:
(2)m+n与p的关系:
(3) T1与T2的关系:
(4)Q与0的关系:
(请用“>”“<”或“=”回答)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com