
题目列表(包括答案和解析)
24、(11)如图某化学实验小组从商店买回的浓硫酸试剂标签的部分内容,该小组在课外资料中获得以下信息:浓硫酸腐蚀性很强,溶于水时释放大量的热,浓硫酸的硫酸分步电离。
|
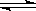 HSO4- + H+
HSO4- + H+
向HSO4- 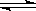 SO42- +
H+
SO42- +
H+
由于试剂瓶口密封签已破损,他们怀疑该硫酸质量分数与标签不符,确定开展研究.
甲认为可以用一种精密仪器测量该溶液的C(H+),若C(H+) =36.8 mol•L-1,该溶液的质量分数为0.98;
乙认为,即使有精密的仪器,甲方案也不行,建议用重量分析法来测。具体设想:取一定体积该硫酸和足量BaCl2反应,过滤、洗涤、干燥沉淀,称量沉淀的质量
丙则建议用“中和滴定”进行测量,设想如下:A、准确量取一定体积的硫酸,并用适量的水稀释;B、往稀释后溶液中滴入2-3滴酚酞;C、用一定浓度的NaOH溶液滴定,直到出现滴定终点为止;D、记录消耗的NaOH溶液的体积。
回答下列问题:。
(1)乙推断“甲同学方案不可行”的理由是: 。
(2)乙方案的关键操作有两点:①确保SO42-完全反应,②洗涤沉淀,确保沉淀不夹杂质。在实验中如何认定SO42-完全反应?
。
(3)如何稀释浓硫酸溶液?
。
(4)丙方案下列操作会使测定结果偏大 。
①在滴定前未用NaOH标准溶液润洗滴定管
②滴定前滴定管尖嘴部分有气泡,滴定后滴定管尖嘴部分气泡消失
③锥形瓶用水洗干净后,未用待测液润洗
④开始时平视读数,滴定完成时俯视读数
(5)丙在实验中,分别取硫酸5.00mL,用5.00mol/L NaOH滴定三次,终点时,得到的NaOH的体积依次为35.65mL、40.62mL、35.55mL,试通过计算该硫酸是否合格.(要计算过程)
23、(9分)现有0.1mol•L-1的纯碱溶液,试用PH试纸测定溶液的PH,其正确的操作是 。纯碱溶液呈碱性的原因(用离子方程式表示)是 - ,你认为该溶液PH的范围一定介于 。
为探究纯碱溶液呈碱性是由CO32-引起的,请你设计一个简单的实验方案。
。
22. 在100℃时,将0.50 mol N2O4气体通入到体积为5.0 L的真空密闭容器中立即出现红棕色,反应进行到2秒时,NO2的浓度为0.02 mol/L,60秒时体系已达平衡,此时容器内压强为开始的1.6倍,下列说法正确的是
A.前2秒以N2O4的浓度变化表示的平均反应速率为0.010 mol/(L·s)
B.在2秒时体系内压强为开始时的1.1倍
C.平衡时体系内含N2O4 为0.25mol
D.平衡时如果压缩容器体积,则可以提高N2O4的转化率
化学试卷
第II卷(非选择题,共76分)
21. 在容积一定的密闭容器中,反应2A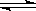 B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
A.正反应是吸热反应,且A不是气态
B.正反应是放热反应,且A是气态
C.其他条件不变,加入少量A,该平衡向正反应方向移动
D. 改变压强对该平衡的移动无影响
20. 已知某溶液中只存在OH--、H+、NH4+、Cl--四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系,其中不可能的是
A、c(Cl--)>c(NH4+)>c(H+)>c(OH--) B、c(Cl--)>c(NH4+)>c(OH--)>c(H+)
C、c(Cl-)>c(H+)>c(NH4+)>c(OH-) D、c(NH4+)>c(Cl-)>c(OH-)>c(H+)
19.把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是
Ca2+(aq)+2OH-(aq).当向悬浊液中加少量生石灰后,若温度保持不变,下列判断正确的是
A.溶液中Ca2+数目减少 B.溶液中c(Ca2+)增大
C.溶液pH值不变 D.溶液pH值增大
18. 在常温下,将PH=11的某碱溶液与PH=3的某酸溶液等体积混合,对此下列说法正确的是 A
A.若所得溶液呈中性,则生成的盐可能为强酸强碱盐
B.若所得的溶液呈碱性,则可能是强碱与弱酸溶液反应
C.若所得溶液呈酸性,则可能是强酸与弱碱溶液反应
D.若所得溶液的PH=5,则可能强碱与弱酸溶液反应
17.常温下设a代表Ba(OH)2,b代表NaOH溶液,c代表NH3·H2O溶液。
下列说法正确的是
A、同物质的量浓度的三种溶液的pH:a>b>c
B、同pH时,三种溶液稀释相同倍数后,pH:a=b<c
C、同pH、同体积的三种溶液消耗同浓度盐酸的体积:a=b=c
D、同pH时,稀释不同倍数、pH仍相同,三种溶液稀释的倍数:a>b>c
16.pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是
A.反应开始时的速率:甲=乙 B.反应所需时间:甲<乙
C.反应开始时,酸的物质的量浓度:甲<乙 D.反应完后溶液的pH值:甲<乙
15. 将相同物质的量浓度的某弱酸HX溶液与NaX溶液等体积混合,测得混合后溶液中c(Na+)>c(X-),则下列关系错误的是
A.c(OH-)>c(H+) B.c(HX)<c(X-)
C.c(X-)+c(HX)=2c(Na+) D.c(HX)+c(H+)=c(Na+)+c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com