
题目列表(包括答案和解析)
练习物质的量浓度相同的下列溶液①(NH4)2CO3 ②(NH4)2SO4 ③NH4HCO3 ④NH4HSO4⑤NH4Cl ⑥NH3·H2O;按c(NH4+)由小到大的排列顺序正确的是( )
A.③⑤④⑥①③ B.⑥③⑤④①② C.⑥⑤③④①② D.⑥③⑤④②①
高考模拟:
1.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:
H2A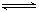 H++HA-,HA-
H++HA-,HA-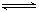 H++A2-
H++A2-
已知相同浓度时的电离度a(H2A)>a(HA-),设有下列四种溶液:
A. 0.01 mol·L-1的H2A溶液
B. 0.01 mol·L-1的NaHA溶液
C. 0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液
D. 0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液
据此,填写下列空白(填代号):
(1) c(H+)最大的是 ,最小的是 。
(2) c(H2A)最大的是 ,最小的是 。
(3) c(A2-)最大的是 ,最小的是 。
答. (1) A;D (2) C;D (3) D;A
5、pH之和等于14的酸和碱溶液的混合:
例:将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈_____性,溶液中c(NH4+)与c(Cl-)的大小关系是___________________;
答案:碱性,c(NH4+)>c(Cl-) ,因为氨水只是少量电离,可见氨水是过量很多,得到的是氯化铵和氨水的混合液,但氨水的量较多
练习18:将pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,所得的混合溶液中,下列关系式正确的是( )
A、 c(Na+)>c(CH3COO-)>c(H+) >c(OH-) B、 c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C、 c(CH3COO-)>c(H+)>c(Na+)>c(OH-) D、c(CH3COO-)>c(Na+)> c(OH-) >c(H+)
练习19:将pH=2的盐酸与pH=12的氨水等体积混合,在所得的混合溶液中,下列关系式正确的是( )
A、c(Cl-)>c(NH4+)>c(OH-)>c(H+) B、c(NH4+)>c(Cl-)> c(OH-)>c(H+)
C、c(Cl-)=c(NH4+)>c(H+)=c(OH-) D、c(NH4+)>c(Cl-)>c(H+)>c(OH-)
4、未指明酸碱的强弱:
例题一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是( )
A.[A-]≥[M+] B.[A-]≤[M+]
C.若MA不水解,则[OH-]<[A-] D.若MA水解,则[OH-]>[A-]
练习17、实验测得常温下0.1mol/L某一元酸(HA)溶液的pH值等于1, 0.1mol/L某一元碱(BOH)溶液里[H+]/[OH-]=10-12、将此两种溶液等体积混合后,所得溶液呈的各离子的浓度由大到小排列的顺序是( )
A.[B+]>[A-]>[OH-]>[H+] B.[A-]>[B+]>[H+]>[OH-]
C.[B+]=[A-]>[H+]=[OH-] D.[B+]>[A-]>[H+]>[OH-]
3、两种物质反应,其中一种有剩余:
例6、把0.02 mol·L-1 HAc溶液与0.01 mol·L-1NaOH溶液等体积混合,则混合液中微粒浓度关系正确的是( )
A、c(Ac-)>c(Na+) B、c(HAc)>c(Ac-)
C、2c(H+)=c(Ac-)+c(HAc) D、c(HAc)+c(Ac-)=0.01 mol·L-1
例7、将0.2 mol·L-1 CH3COOK 与0.1 mol·L-1盐酸等体积混合后,溶液的pH<7,则溶液中下列微粒的物质的量浓度的关系正确的是( )
A、c(CH3COO-)=c(Cl-)=c(H+)>c(CH3COOH)
B、c(CH3COO-)=c(Cl-)>c(CH3COOH)>c(H+)
C、c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)
D、c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
练习16:将0.4mol/LNH4Cl溶液和0.2mol/LNaOH溶液等体积混合后,溶液中下列微粒的物质的量关系正确的是( )
A 、c(NH4+)=c(Na+)=c(OH-)>c(NH3·H2O)
B、c(NH4+)=c(Na+)>c(NH3·H2O) >c(OH-)>c(H+)
C、c(NH4+)>c(Na+)>c(OH-)>c(NH3·H2O)
D、c(NH4+)>c(Na+)>c(NH3·H2O) >c(OH-)>c(H+)
2、两种物质恰好完全反应:
例5:100 mL 0.1 mol·L-1 醋酸与50 mL 0.2 mol·L-1 NaOH溶液混合,在所得溶液中( )
A、c(Na+)>c(CH3COO-)>c(OH-)>c(H+) B、c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C、c(Na+)>c(CH3COO-)>c(H+)=c(OH-) D、c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
练习14:在甲酸溶液中加入一定量NaOH溶液,恰好完全反应,对于生成的溶液,下列判断一定正确的是( )
A、c(HCOO-)<c(Na+) B、c(HCOO-)>c(Na+)
C、c(OH-)>c(HCOO-) D、c(OH-)<c(HCOO-)
练习15:等体积等浓度的醋酸与NaOH溶液相混合,所得溶液中离子浓度由大到小的顺序是( )
A、c(Na+)>c(Ac-)>c(OH-)>c(H+) B、c(Na+)=c(Ac-)>c(OH-)>c(H+)
C、c(Na+)>c(OH-)>c(Ac-)>c(H+) D、c(Na+)>c(OH-)>c(H+)>c(Ac-)
如果一定量的醋酸和氢氧化钠混合后,溶液的pH=7,则各离子浓度的关系为( )
A、c(Na+)>c(Ac-) B、c(Na+)=c(Ac-)
C、c(Na+)<c(Ac-) D、c(OH-)>c(H+)
1、两种物质混合不反应:
例4、用物质的量都是0.1 mol的CH3COOH与CH3COONa配成1 L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液下列判断正确的是( )
A、c(H+)>c(OH-) B、c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1
C、c(CH3COOH)>c(CH3COO-) D、c(CH3COO-)+c(OH-)=0.1 mol·L-1
练习13、CH3COOH与CH3COONa等物质的量混合配制成稀溶液,pH值为4.7,下列说法错误的( )
A、CH3COOH的电离作用大于CH3COONa的水解作用
B、CH3COOH的存在抑制了CH3COONa的水解
C、CH3COONa的水解作用大于CH3COOH的电离作用
D、CH3COONa的存在抑制了CH3COOH的电离
例2、H2S溶液中,各离子浓度大小关系为________________________________________,
例3、Na2S溶液中有哪些微粒?_________________________________________________,
例4、在2mol/L的CH3COONa溶液中,存在哪些平衡?存在哪些守恒关系?
练习7: 在NH4Cl溶液中,离子浓度大小排队正确的是( )
A、c(NH4+)> c(Cl-)> c(OH-)> c(H+) B、c(Cl-)> c(NH4+)> c(OH-)> c(H+)
C、c(Cl-)>c(NH4+)> c(H+)> c(OH-) D、 c(NH4+)> c(Cl-)> c(H+)> c(OH-)
练习8:常温下,下列关于0.1mol/LNH4Cl溶液的说法正确的是( )
①c(NH4+)=0.1mol·L-1 ; ②溶液中 c(H+)· c(OH-)=1.0×10-14 ;
③水电离出来的 c(H+)= c(OH-); ④溶液的pH=1 ;
⑤ c(OH-)= c(NH4+)+ c(H+)- c(Cl-); ⑥升高温度,溶液的pH增大;
⑦加热蒸干溶液,将得不到固体物质; ⑧ c(NH4+)+ c(NH3·H2O)=0.1mol·L-1;
⑨ c(OH-)+ c(NH3·H2O)= c(H+); ⑩ NH4Cl水解的离子方程式为: NH4++OH-== NH3·H2O、
练习9: Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
A、c(Na+)>c(S2-)>c(OH-)>c(HS-) B、c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
C、c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) D、c(OH-)=c(H+) + c(HS-)
练习10、在0.1 mol·L-1的NaHCO3溶液中,下列关系式正确的是( )
A、c(Na+)>c(HCO3-)>c(H+)>c(OH-) B、c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
C、c(Na+)=c(HCO3-)>c(OH-)>c(H+) D、c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-)
练习11、已知某温度下0.1mol·L-1的NaHB(强电解质)溶液中c(H+)> c(OH-),则下列有关说法或关系式一定正确的是( )
①HB-的水解程度小于HB-的电离程度; ②c(Na+)=0.1mol·L-1 ≥ c(B2-);
③溶液的pH=1; ④ c(Na+)= c(HB-)+2 c(B2-)+ c(OH-)、
A、①② B、②③ C、②④ D、①②③
练习12、已知某酸的酸式盐NaHY的水溶液的pH=8,则下列说法中正确的是( )
A、在Na2Y、NaHY、H2Y的溶液中,阴离子的种类不同
B、NaHY的溶液中,离子浓度大小顺序为:c(Na+)> c(Y-)> c(HY-)> c(OH-)> c(H+)
C、HY-的水解离子方程式为:HY-+H2O Y-+H3O+
Y-+H3O+
D、相同物质的量浓度的Na2Y和NaHY溶液,前者的pH大于后者
例1、100℃时纯水电离出的氢离子是25℃纯水电离出的氢离子的多少倍(已知:100℃时Kw=1×10-12;25℃时Kw=1×10-14( )
A 10-2 B 2倍 C 102 D 10倍
练习1:25℃时PH=3的盐酸溶液中由水电离出c(H+)是PH=5的盐酸溶液中由水电离出的c(H+)的多少倍( )
A 103 B 10-2 C 10-3 D 2
练习2:常温下某溶液由水电离出的c(H+)=1×10-11mol/L,则该溶液的PH值可能等于( )
A 11 B 3 C 8 D 7
练习3:25℃时,PH=11的NaOH溶液和NaCN溶液中,由水电离出的c(H+)的关系( )
A 相等 B 后者是前者的11倍 C 后者是前者的108 D前者是后者的108
练习4:将固体苛性钠溶于水配成100mL溶液,当溶液中由水本身电离产生的
c(OH-)=1×10-13mol/l,则加入的苛性钠的质量为( )
A 0.8g B 0.4g C 4g D 40g
练习5:下列四种溶液(1)pH=0的盐酸溶液 (2)0.1mol/L的盐酸溶液 (3)0.01mol/L的NaOH (4)pH=11的NaOH溶液由水电离出的c(H+)浓度之比( )
A 1:10:100:1000 B 0:1:11:11
C 14:13:12:11 D 100;10:1:0
练习6:在由水电离出的c(H+)=10-13mol·L-1的溶液中,一定能大量共存的离子组是( )
A、 K+、Fe2+、 Br-、 NO3- B、 Ba2+、Na+、Cl-、 NO3-
C、 NH4+、Na+、HCO3-、SO42- D、 Na+、Al3+、NO3-、Cl-
29.c(HNO3)=2 mol/L , c(H2SO4)= 3 mol/L 。
28.(1) 否,若a=3,则b=6,溶液显酸性,与题意不符,故a≠3 。
(2)否,若a=5,c(H+)a=10-5mol/L,则b=10,c(OH-)b = 10-4mol/L ,
Va / Vb=c(OH-)b / c(H+)a > 1 , 不符合题意,故a≠5 。
(3)7/2<a<14/3 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com