
题目列表(包括答案和解析)
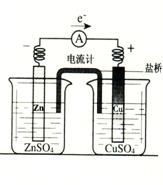
22、有关如右图所示原电池的叙述,正确的是(盐桥中装有含琼胶的KCl饱和溶液)
A.反应中,盐桥中的K+会移向CuSO4溶液
B.取出盐桥后,电流计依然发生偏转
C.铜片上有气泡逸出
D.反应前后铜片质量不改变
21、常温下,现有PH=2的某酸HX溶液和PH=12某碱YOH溶液,两溶液混合后,溶液的pH小于7。下表中判断合理的是
|
编号 |
HX |
YOH |
溶液的体积关系 |
|
A |
强酸 |
强碱 |
V(HX)=V(YOH) |
|
B |
强酸 |
强碱 |
V(HX)<V(YOH) |
|
C |
强酸 |
弱碱 |
V(HX)=V(YOH) |
|
D |
弱酸 |
强碱 |
V(HX)=V(YOH) |
20、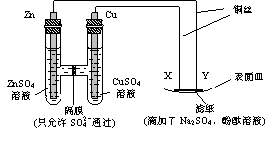 如图所示,下列叙述正确的是
如图所示,下列叙述正确的是
A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
19、已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol/L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中一定正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C.c(RO32-)+c(HRO3-)+c(H2RO3)=c(Na+)
D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
18、汽车的启动电源常用铅蓄电池,电池反应如下:
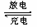 PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是
PbO2 + Pb + 2H2SO4 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是
A.PbO2放电时是电池的负极,充电时是电池的阳极。
B.负极的电极反应式为:Pb + SO – 2e – = PbSO4
– 2e – = PbSO4
C.放电时,PbO2得电子,被氧化
D.电池放电时,溶液酸性增强
17、用0.01mol/L的NaOH溶液完全中和pH=3的下列溶液各100mL。需要NaOH溶液的体积最大的是
A、盐酸 B、硫酸 C、高氯酸 D、醋酸
16、常温,某溶液中由水电离产生的c(H+)、c(OH-)满足c(H+)·c(OH-)=10-24,则下列各组离子在该溶液中一定可以大量共存的是
A.K+、Na+、AlO2-、Cl- B.Na+、Cl-、SO42-、HCO3-
C.NH4+、Na+、NO3-、SO42- D.Ba2+、Na+、Cl-、NO3-
15、一定条件下反应N2+3H2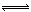 2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是
A.加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等
2NH3达平衡,当单独改变下述条件后有关叙述一定错误的是
A.加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等
B.加压,v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数
C.降温,v(正)和v(逆)都减少,且v(正)减少倍数大于v(逆)减少倍数
D.增加c(N2),v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数
14、已知NaHSO4在水中的电离方程式为:NaHSO4===Na++H++SO 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,
不正确的是
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
13、
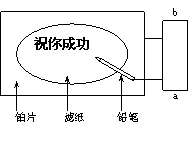 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
 A.铅笔端作阳极,发生还原反应
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是电源的负极,b点是电源的正极
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com