
题目列表(包括答案和解析)
19.(6分)在25℃时,氢氟酸、醋酸和次氯酸的电离常数分别是3.5×10-4、1.8×10-5、3.0×10-8。请推测:它们的酸性由强到弱的顺序为______________________,相同浓度的溶液中,氢离子浓度最大的是__________,电离度最小的是_______;相同浓度的氟化钠溶液、醋酸钠溶液、次氯酸钠溶液pH的从大到小顺序:_____________________________。
18.(6分)在常温下, 200 mL含有1×10-3 mol的钡离子的氢氧化钡溶液pH值为__________。将此溶液与pH=3的盐酸混合,使其混合溶液的pH=7,应取氢氧化钡溶液和盐酸的体积之比是________。
17.(4分)请设计两种实验方案,探究氢氧化钠和一水合氨的碱性强弱。
16.下图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是 ( )
 A.④>②>①>③
A.④>②>①>③
B.②>①>③>④
C.④>②>③>①
D.③>②>④>①
15.如图所示装置中,a、b都是惰性电极,烧杯中为电解质溶液。通电一段时间后,a极附近呈红色。下列说法中正确的是:( )

A.a是阳极,b是阴极
B.X是负极,Y是正极
C.CuSO4溶液的pH减小
D.a极产生氯气,b产生氢气
14.在1L浓度为c mol/L的弱酸HA溶液中,HA、A- 和H+三种粒子的物质的量之和为 nc mol,则该弱酸的电离度是( )
A.100n% B.c¸n´100% C.100(n-1)% D.n%
13.在Na2CO3溶液中存在如下水解平衡CO32-+H2O  HCO3-+OH-
HCO3-+OH-
和HCO3-+H2O  H2CO3+OH- ,往此溶液中加入下列物质,能使平衡向逆反应方向移动,且溶液的pH减小的是( )
H2CO3+OH- ,往此溶液中加入下列物质,能使平衡向逆反应方向移动,且溶液的pH减小的是( )
A.CaCl2溶液 B.盐酸 C.NaOH溶液 D.Al2(SO4)3溶液
12. 常温下,0.1 mol/L某一元酸(HA)溶液中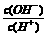 =1×10-8,下列叙述正确的是( )
=1×10-8,下列叙述正确的是( )
A.溶液中水电离出的c(H+)=10-10 mol/L B.该一元酸(HA)是强酸
C.加水稀释,溶液的c(OH-)增大 D.溶液中c(H+)+c(A-)=0.1 mol/L
11.用物质的量都是 0.1 mol 的CH3COOH和CH3COONa 配制成 1 L混合溶液。已知其中c(CH3COO-)大于c(Na+)。对于该混合溶液下列判断正确的是( )
A.c(H+)<c(OH-) B.c(CH3COOH)+c(CH3COO-)=0.1mol/L
C.c(CH3COOH)< c(CH3COO-) D.c(CH3COO-)+c(OH-)=0.2mol/L
10.在下列各组离子中,能大量共存的是:( )
A.Ag+、NO3-、Na+、Cl- B.K+、HCO3-、Cl-、Al3+
C.NO3-、Fe2+、H+、Br- D.K+、Cl-、SO42-、NH4+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com