
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
6ЁЂдквНбЇЁЂШеГЃЩњЛюжаГЃМћЕФШмвКЃКЂйИЃЖћТэСж ЂквНгУЯћЖООЦОЋ ЂлЩњРэбЮЫЎ ЂмЪГДзЃЛетаЉШмвКжаЕФШмжЪжЪСПЗжЪ§гЩДѓЕНаЁЫГађЮЊ (ЁЁЁЁ )
ЁЁЁЁЁЁЁЁ A.ЂйЂкЂлЂмЁЁЁЁЁЁ B.ЂйЂкЂмЂлЁЁЁЁ ЁЁЁЁЁЁ C.ЂкЂмЂйЂлЁЁ ЁЁЁЁЁЁ D.ЂкЂйЂмЂл
5ЁЂввДМЗжзгжаИїЛЏбЇМќШчЭМЫљЪОЃЌЖдввДМдкИїжжЗДгІжагІЖЯСбЕФМќЫЕУїВЛе§ШЗЕФЪЧ
A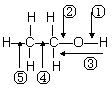 ЃЎКЭН№ЪєФЦзїгУЪБЃЌМќЂйЖЯСб
ЃЎКЭН№ЪєФЦзїгУЪБЃЌМќЂйЖЯСб
BЃЎКЭХЈСђЫсЙВШШжС170 ЁцЪБЃЌМќЂкКЭЂнЖЯСб
CЃЎКЭввЫсЁЂХЈСђЫсЙВШШжЦввЫсввѕЅЪБЃЌМќЂкЖЯСб
DЃЎдкЭДпЛЏЯТКЭбѕЦјЗДгІЪБЃЌМќЂйКЭЂлЖЯСб
4ЁЂЯТСаЫЕЗЈжаДэЮѓЕФЪЧ: (ЁЁЁЁ )
ЂйЛЏбЇаджЪЯрЫЦЕФгаЛњЮяЪЧЭЌЯЕЮя
ЂкЗжзгзщГЩЯрВювЛИіЛђМИИіCH2дзгЭХЕФгаЛњЮяЪЧЭЌЯЕЮя
ЂлШєЬўжаЬМЁЂЧтдЊЫиЕФжЪСПЗжЪ§ЯрЭЌЃЌЫќУЧБиЖЈЪЧЭЌЯЕЮя
ЂмЛЅЮЊЭЌЗжвьЙЙЬхЕФСНжжгаЛњЮяЕФЮяРэаджЪгаВюБ№ЃЌЕЋЛЏбЇаджЪБиЖЈЯрЫЦ
A. ЂйЂкЂлЂмЁЁЁЁ B. жЛгаЂкЂлЁЁЁЁ C. жЛгаЂлЂмЁЁЁЁЁЁ D. жЛгаЂйЂкЂл
3ЁЂЯжгаЯТСаЮяжЪЃКЂйЯЫЮЌЫиЁЁ ЂкМзЫсМзѕЅЁЁ ЂлЕэЗлЁЁ ЂмМзШЉЁЁ ЂнБћЫсЁЁ ЂоШщЫс(ІС-єЧЛљБћЫс)
ЁЁ ЂпввЖўДМЁЁ ЂрввЫсЁЃЦфжаЃЌЗћКЯCn(H2O)mЕФзщГЩЃЌЕЋВЛЪєгкЬЧРрЕФЪЧЁЁЁЁ (ЁЁЁЁ )
ЁЁЁЁ ЁЁ AЃЎЂкЂлЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂйЂлЂмЂпЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎЂкЂмЂоЂр ЁЁЁЁЁЁЁЁЁЁ DЃЎЂкЂмЂнЂр
2ЁЂЯТСагаЙиЛЏбЇгУгяе§ШЗЕФЪЧ (ЁЁЁЁ )
AЃЎввДМЁЂввЖўДМЁЂБћШ§ДМЛЅЮЊЭЌЯЕЮяЃЌЭЌЯЕЮяжЎМфВЛПЩФмЮЊЭЌЗжвьЮяЬх
BЃЎ2008ФъББОЉАТдЫЛсНБХЦ--ЁАН№ЯтгёЁБНБХЦгёЕФЛЏбЇГЩЗжЖрЮЊКЌЫЎИЦУОЙшЫсбЮЃЌШчЃКCa2Mg5Si8O22(OH)2ПЩгУбѕЛЏЮяБэЪОЮЊЃК2CaOЁЄ5MgOЁЄ8SiO2ЁЄH2O
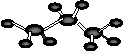 CЃЎДЮТШЫсЕФНсЙЙЪНЮЊЃКH-Cl-OЁЁ
CЃЎДЮТШЫсЕФНсЙЙЪНЮЊЃКH-Cl-OЁЁ
DЃЎБћЭщЗжзгЕФБШР§ФЃаЭЪОвтЭМЃК
1ЁЂ2007Фъ10дТ10ШеЕТЙњИёЙўЕТЁЄАЃЬиЖћвђдкБэУцЛЏбЇбаОПСьгђзїГіПЊЭиадЙБЯзЖјЛёЕУХЕБДЖћЛЏбЇНБЁЃдкЮяжЪБэУцЫљЗЂЩњЕФвЛЧаЮяРэЛЏбЇЯжЯѓГЦЮЊБэУцЯжЯѓЃЌЖјбаОПИїжжБэЯжЯжЯѓЪЕжЪЕФПЦбЇГЦЮЊБэУцЛЏбЇЁЃБэУцЛюадМСжИЛюдОгкБэУцКЭНчУцЩЯОпгаМЋИпЕФНЕЕЭБэУцЁЂНчУцеХСІЕФФмСІЕФвЛРрЮяжЪЁЃІС-ЯЉЛљЛЧЫсФЦЪЧвЛжжГЃМћЕФБэУцЛюадМСЃЌ ЦфНсЙЙМђЪНЮЊRCH=CH(CH2)nSO3NaЃЌГЃгУзїЯДЕгМСЃЌгаЙиЦфа№Ъіе§ШЗЕФЪЧ (ЁЁЁЁ )
AЁЂІС-ЯЉЛљЛЧЫсФЦФбШмгкЫЎЁЁЁЁЁЁ BЁЂІС-ЯЉЛљЛЧЫсФЦжаЁА-SO3Na ЁБЮЊдїЫЎЛљ
CЁЂІС-ЯЉЛљЛЧЫсФЦЫЎШмвКЯдЫсадЁЁ DЁЂІС-ЯЉЛљЛЧЫсФЦФмЪЙфхЫЎЭЪЩЋ
23ЃЎ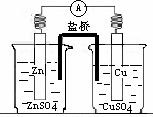 (9Зж)(1)гвЭМЮЊЭаПдЕчГиЕФзАжУЧыЛиД№ЃК
(9Зж)(1)гвЭМЮЊЭаПдЕчГиЕФзАжУЧыЛиД№ЃК
ЭЪЧЁЁЁЁ МЋЃЌЭЦЌЩЯВњЩњЁЁЁЁЁЁЁЁЁЁ ЃЌ
ЕчМЋЗДгІЪНЮЊ_____________________ЃЛ
аПЮЊЁЁЁЁ МЋЃЌЕчМЋЗДгІЪНЮЊ________________ЃЛ
ЕчГиЗДгІЪНЮЊ__________________________ЁЃ
(2) Чт-бѕШМСЯЕчГиЃКЫќЕФИКМЋЪЧЖрПзЕФФјЕчМЋЃЌе§МЋЮЊИВИЧбѕЛЏФјЕФФјЕчМЋЃЌЕчНтжЪШмвКЪЧKOHШмвКЃЌдкИКМЋЭЈШыH2ЃЌе§МЋЭЈШыO2ЃЌЕчМЋЗДгІЃКИКМЋЃКЁЁЁЁЁЁЁЁЁЁ е§МЋЃК ЁЁЁЁЁЁЁЁЕчГиЗДгІЪНЮЊ__________________________ЁЃ
22.(10Зж)
(1)ЛЏбЇЦНКтГЃЪ§KБэЪОПЩФцЗДгІЕФНјааГЬЖШЃЌKжЕдНДѓЃЌБэЪО________ЃЌKжЕДѓаЁгыЮТЖШЕФЙиЯЕЪЧЃКЮТЖШЩ§ИпЃЌKжЕ_______________(ЬюЁАвЛЖЈдіДѓЁБЁАвЛЖЈМѕаЁЁБЛђЁАПЩФмдіДѓвВПЩФмМѕаЁЁБ)ЁЃ
(2)дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк800ЁцЪБЗЂЩњШчЯТЗДгІЃК
CO(g)+H2O (g)  CO2(g)+H2 (g)ЁЁЁїHЃМ0
CO2(g)+H2 (g)ЁЁЁїHЃМ0
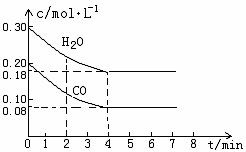
COКЭH2OЮяжЪЕФСПХЈЖШБфЛЏШчЯТЭМ(a)ЫљЪОЃЌдђЃК
Ђй 0Ѓ4minМфЦНОљЗДгІЫйТЪv(CO)ЃН________ mol•LЃ1•minЃ1ЁЁЁЁЁЁ ЁЁ
Ђкдк800ЁцЪБИУЗДгІЕФЛЏбЇЦНКтГЃЪ§KЃН___________________________(вЊЧѓаДГіБэДяЪНМАЪ§жЕ)ЃЛCOЕФзЊЛЏТЪЃН______________ЁЃ
ЁЁЁЁЁЁ ЭМ(a)
Ђлдк800ЁцЪБЃЌШєЗДгІПЊЪМЪБДЫШнЦїжаCOКЭH2OЕФХЈЖШЗжБ№ЮЊ0.20 mol/LКЭ0.80 mol/LЃЌдђДяЕНЦНКтЪБCOзЊЛЏЮЊCO2ЕФзЊЛЏТЪЪЧЃК______________________ЁЃ
21.(7Зж)ЧтбѕЛЏБЕЪЧвЛжжЪЙгУЙуЗКЕФЛЏбЇЪдМСЁЃФГПЮЭтаЁзщЭЈЙ§ЯТСаЪЕбщВтЖЈФГЪдбљжаBa(OH)2ЁЄnH2OЕФКЌСПЁЃ
(1)ГЦШЁ3.50gЪдбљШмгкеєСѓЫЎХфГЩ100mLШмвКЃЌДгжаШЁГі10.0mLШмвКгкзЖаЮЦПжаЃЌМг2ЕЮжИЪОМСЃЌгУ0.100mol/LHClБъзМШмвКЕЮЖЈжСжеЕуЃЌЙВЯћКФБъзМвК20.0mL(дгжЪВЛгыЫсЗДгІ)ЃЌЧѓЪдбљжаЧтбѕЛЏБЕЕФЮяжЪЕФСПЁЃ
(2)СэШЁ5.25gЪдбљМгШШжСЪЇШЅШЋВПНсОЇЫЎ(дгжЪВЛЗжНт)ЃЌГЦЕУжЪСПЮЊ3.09gЃЌЧѓBa(OH)2ЁЄnH2OжаЕФnжЕЁЃ
(3)ЪдбљжаBa(OH)2ЁЄnH2OЕФжЪСПЗжЪ§ЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
20.(10Зж)
(1)Fe2(SO4)3ЕФЫЎШмвКГЪЁЁЁЁЁЁЁЁ (ЬюЁАЫсЁБЁЂЁАжаЁБЁЂЁАМюЁБ)адЃЌГЃЮТЪБЕФpH ЁЁЁЁЁЁ7(ЬюЁА>ЁБЁЂЁА=ЁБЁЂЁА<ЁБ)ЃЌдвђЪЧ(гУРызгЗНГЬЪНБэЪО)ЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛЪЕбщЪвдкХфжЦFe2(SO4)3ШмвКЪБЃЌГЃНЋFe2(SO4)3ЙЬЬхЯШШмгкНЯХЈЕФЁЁЁЁЁЁ жаЃЌШЛКѓдйгУеєСѓЫЎЯЁЪЭЕНЫљашЕФХЈЖШЃЌвдЁЁЁЁЁЁЁЁ ЁЁ(ЬюЁАДйНјЁБЁЂЁАвжжЦЁБ)ЦфЫЎНтЁЃдкХфжЦСђЛЏФЦШмвКЪБЃЌЮЊСЫНЕЕЭЦфЫЎНтГЬЖШЃЌПЩвдМгШыЩйСПЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)ЧыздМКЩшМЦЪЕбщЬНОПЃКЮТЖШЖдFe2(SO4)3ЫЎНтЦНКтЕФгАЯьЁЃ(вЊЧѓаДГіЪЕбщВНжшЁЂЯжЯѓКЭНсТл)
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com