
题目列表(包括答案和解析)
2.下列符号中,元素符号的书写正确的是( )
A.钙:CA B.铝:aL C.镁:mg D.铁:Fe
思路解析:书写元素符号时,用拉丁文名称第一个大写字母表示,若几种元素符号的第一个字母相同时,则再附加一个小写字母表示。
答案:D
1. ____________________________________________叫单质。
_____________________________________________________叫化合物。
_____________________________________________________叫元素符号。
答案:如氢气、氧气等,只由一种元素组成的物质 如水、二氧化碳等,由两种或两种以上元素组成的物质 每种元素都采用国际上规定的统一的符号来表示,这种统一的符号
8.原子是由原子核和电子构成的。原子核在原子中所占体积极小,其半径约为原子半径的十万分之一,因此,相对而言,原子里有很大的空间。α微粒是带两个单位正电荷的氦原子。1911年,科学家用一束平行高速运动的α微粒轰击金箔时(金原子的核电荷数为79,相对原子质量为197),发现三种实验现象:
(1)有一小部分α微粒改变了原来的运动路径,原因是α微粒途经金原子核附近时,受到斥力而稍微改变了运动方向。
(2)大多数α微粒不改变原来的运动方向,原因是____________________________________。
(3)极少数α微粒被弹了回来,原因是_____________________________________________。
思路解析:此题为信息给予题,考查对原子的内部结构的微观理解程度。该题命题灵活、新颖。原子中原子核所占体积极小,其半径约为原子半径的十万分之一,相对而言,原子中电子运动有很大的空间,但原子的质量主要集中在原子核上,即原子核中正电荷密集、质量大、体积很小。当用带两个单位正电荷的氦原子去轰击正电荷、质量都很大的金原子时,α微粒能顺利通过原子内相对较大的空间和原子间空隙,如撞击到原子核时,则被弹回。
答案:(2)原子内、原子间有空隙 (3)α微粒撞击了金原子核而被弹回(或α微粒撞击了带正电荷、质量大、体积很小的金原子核而被弹回)
1.66×10-27 kg×80=1.328×10-25 kg
答案:1.328×10-25
7.碳12原子的质量为1.993×10-26 kg,某原子的相对原子质量是80,则该原子的实际质量是_________kg。
思路解析:本题考查的是原子的质量和相对原子质量关系的计算。解题的关键是要搞清原子的质量和相对原子质量二者的区别和联系。
(1)相对原子质量不是原子的实际质量,而是一个比值。
(2)相对原子质量的标准是一个C-12原子质量的1/12,其他原子的质量跟它相比较所得的比值就是该种原子的相对原子质量。
C-12原子质量的1/12=1.933×10-26 kg/12≈1.66×10-27 kg
某原子的相对原子质量为80,则该原子的质量为:
6.(经典回放)为形象展示水分解的微观过程,某同学制作了一些模型,表示相应的微观粒子。其中表示水分解过程中不能再分的微粒是( )
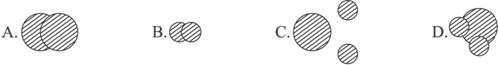
思路解析:用直观模型展示微观粒子,让学生从宏观的角度感受化学变化的微观世界。因为一个水分子是由两个氢原子和一个氧原子构成的,结合所示模型分析,可知D模型表示一个水分子,进而推出A表示一个氧分子,B表示一个氢分子,C表示一个氧原子、两个氢原子。又因为在化学反应中,分子可分,原子不能再分,所以水分解过程中不能再分的微粒应是C选项展示的原子。
答案:C
5.(2010福建福州中考)根据钠原子结构示意图 ,判断下列说法错误的是( )
,判断下列说法错误的是( )
A.钠原子核外有3个电子层 B.钠原子在化学反应中容易得到电子
C.钠原子最外层只有一个电子 D.钠原子的核电荷数为11
思路解析:钠原子的最外层电子数为1,在化学反应中易失去1个电子,使次外层变为8个电子的相对稳定结构。
答案:B
4.“神舟”五号不仅将杨利伟送上太空,实现了亿万中国人的梦想,同时还承担着其他的科研任务。比如探索宇宙中可能存在完全由反微粒构成的物质--反物质。物质与反物质相遇会发生“湮灭”现象,释放出巨大的能量,在能源研究领域中前景可观。正电子、负质子等都是反微粒。它们与通常所说的电子、质子相比较,质量相等但电性相反。请你推测,反氢原子的结构可能是 ( )
A.由一个带正电荷的质子与一个带负电荷的电子构成
B.由一个带负电荷的质子与一个带正电荷的电子构成
C.由一个带正电荷的质子与一个带正电荷的电子构成
D.由一个带负电荷的质子与一个带负电荷的电子构成
思路解析:根据所给信息,反氢原子是由1个反质子和反电子构成的,反质子带一个单位负电荷,反电子带一个单位正电荷。
答案:B
3.(经典回放)英国科学家道尔顿最先确立了原子学说,他的中心论点主要有:①原子是不能再分的微粒;②原子是微小的实心球;③同种元素的原子,其性质和质量都相同。而现代科学实验表明:同种元素的原子内部有相同的质子数和不一定相同的中子数。从现代的观点看,你认为道尔顿的三个论点中,不确切的是( )
A.① B.①③ C.②③ D.①②③
思路解析:①原子是可以再分的,且并不是实心球;②由于原子的质量主要集中在原子核上,质子和中子的质量决定了原子的质量,而自然界中有许多质子数相等、中子数不等的原子,如C-12和C-14,原子核内均有6个质子,前者原子核中有6个中子,后者原子核中有8个中子。
答案:D
2.下列关于原子的叙述正确的是( )
A.原子是不能再分的微粒 B.一切物质都是由原子直接构成的
C.一切原子的原子核由质子和中子构成 D.原子核内质子数必等于核外电子数
思路解析:原子在化学变化中不可分,但在其他变化(核反应)中可以再分,原子是由原子核和核外电子构成的,所以A不对。有些物质是由分子构成的,如氧气、氨气、二氧化碳等,有的物质是由原子直接构成的,如铜、铝、汞等,所以B不对。绝大多数原子的原子核都是由质子和中子构成的,但是氢原子的原子核内没有中子,所以C不对。原子呈电中性决定了质子数必须等于核外电子数,所以D对。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com