
题目列表(包括答案和解析)
2.有6种物质:①甲烷;②苯;③聚乙烯;④苯乙烯;⑤丁炔;⑥邻二甲苯。既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是
A.③④ B.④⑤ C. ④⑤⑥ D. ③④⑤
1.20世纪末,由中国学者和美国科学家共同合成了世界上最大的碳氢分子,其一个分子由1334个碳原子和1146个氢原子构成.关于此物质,则其分子中含有的碳碳三键最多有
A.281 B.148 C.149 D.150
26.有两种烃的蒸气,B对A的相对密度为3,它们等物质的量混合后完全燃烧,所消耗的O2为混合气体的5倍(同温同压下体积比),两烃分别燃烧得到生成物的质量比均为m(CO2)∶m(H2O)= 44∶9,求这两种烃的分子式
25.(4分)若使1 mol CH4与Cl2在一定条件下发生取代反应,假设生成的四种氯代物的物质的量相同,需Cl2物质的量为 mol ;当恢复至室温时,生成气体的总物质的量为 mol
24.(7分)⑴通常烷烃由相应的烯烃经催化加氢得到,但是分子式为C5H12的烷烃A却不能由任何C5H10的烯烃加氢得到,而A的一种同分异构体B,可由三种相应的烯烃催化加氢得到。则A和B的结构简式分别为 、
⑵某无色透明溶液,跟金属铝反应放出H2,在原溶液中可能存在下列离子:Mg2+、Cu2+、Ba2+、Ag+、H+、SO42-、SO32-、HCO3-、OH-、NO3-。当金属铝与其作用生成AlO2-时,在原溶液中一定大量存在的离子是 ,
可能还大量存在 离子。
23. (4分)可逆反应: aA(g) + bB
(g) cC(g)+ dD(g) 试根据图回答问题
(4分)可逆反应: aA(g) + bB
(g) cC(g)+ dD(g) 试根据图回答问题
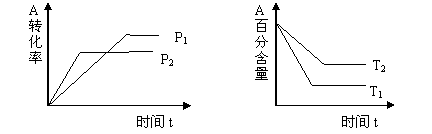

⑴ 压强P1 P2 (填“<”“>”或“=”)
⑵ a + b c+ d (填“<”“>”或“=”)
⑶ 温度T1 T2 (填“<”“>”或“=”)
⑷ 该反应的正反应为 (填“吸热”或“放热”)
22.(12分)混合物A由KAl(SO4)2 、Al2O3和Fe3O4组成,在一定条件下可 实现如下图所示的物质之间的转化
实现如下图所示的物质之间的转化
⑴反应①的离子方程式
反应②的离子方程式
⑵ 将沉淀C加入过量的稀盐酸中充分反应,简述所得溶液中Fe3+的检验方法 有关检验的离子方程式
⑶ 利用⑵中的溶液制取FeCl3∙6H2O晶体,设计流程如下:

 溶液 FeCl3溶液 FeCl3∙6H2O晶体
溶液 FeCl3溶液 FeCl3∙6H2O晶体
① 步骤Ⅰ中通入Cl2的作用(用化学方程式说明)
② 步骤Ⅱ中从FeCl3溶液中得到FeCl3∙6H2O晶体的主要操作包括
③该流程中需要保持盐酸过量,主要原因是(结合离子方程式简要说明)
21.(4分)有MgCl2和Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到沉淀量与加入的NaOH溶液的体积关系如图所示

⑴写出由a点到b点时反应的离子方程式
⑵溶液中C(Cl-)与C(SO42-)之比为
20.(11分)下图是某同学设计的
实验室用酒精和浓硫酸混合制乙烯
的实验装置图,回答下列问题
⑴ 指出装置中存在的明显错误是
⑵在反应容器a中发生的化学反应方程式是 ;
反应中浓硫酸的作用是
⑶加热混合液时,应使液体温度迅速升到170℃,原因是
⑷在进行乙烯性质实验前,先将产生的气体通过质量分数为10%的NaOH溶液,此项操作的目的是
⑸将用NaOH溶液洗涤后的气体分别通过溴的四氯化碳溶液和酸性高锰酸钾溶液中,溶液颜色均可褪去,使其褪色的反应类型 ,其中使溴的四氯化碳溶液褪色的化学反应方程式为
19.(5分)化学电池在通讯、交通及生活中有着广泛的应用。如图装置由镁条、铝条和某种电解质溶液组成。
⑴若电解质溶液为稀硫酸,则原电池的负极反应为 ,正极上的现象为
 ⑵若电解质溶液为较浓的NaOH溶液,此装置能否构成原电池
(填“能”或“否”,若填“否”,则后面不需作答)。若能构成原电池,则外电路电子从 流向
⑵若电解质溶液为较浓的NaOH溶液,此装置能否构成原电池
(填“能”或“否”,若填“否”,则后面不需作答)。若能构成原电池,则外电路电子从 流向
 (填“Mg”或“Al”).当线路中有0.6 mol电子通过时,消耗负极材料的质量是 g。
(填“Mg”或“Al”).当线路中有0.6 mol电子通过时,消耗负极材料的质量是 g。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com