
题目列表(包括答案和解析)
26.(5分)(1) 5.3 (2) 容量瓶(250mL) 、 胶头滴管
(3) 5.6L 、2 mol·L-1
25.(5分)(1)SiO2
(2)3Si+2N2
 Si3N4
Si3N4
3SiCl4+2N2+6H2 Si3N4+12HCl
Si3N4+12HCl
24.(5分)
(1)C7H7O2N 羧基 (2)酸
(3)R-COOH+Na2CO3=R-COONa+H2O+CO2↑
(4)
28.(10分)某同学将一小片铜块投入足量的浓硝酸后,再将生成的气体A通过水洗得到标准状况下11.2L的气体B。
(1)气体B的化学式是 ;
(2)将铜片投入浓硝酸中可观察到的现象是溶液由无色变成 色,同时生成 色的气体;
(3)通过计算求出铜片的质量。
高中期末考试评分标准
27. (6分)今有中学化学常见的五种物质,他们在一定条件下有如图所示的转化关系。写出一个符合下列条件的反应Ⅰ的化学方程式。
(6分)今有中学化学常见的五种物质,他们在一定条件下有如图所示的转化关系。写出一个符合下列条件的反应Ⅰ的化学方程式。
(1)若A为金属单质,B为非金属单质:
;
(2)若A和B均为金属单质:
;
(3)若A为化合物,B为金属单质:
。
26.(5分)某同学欲配制250 mL 2 mol·L-1 的碳酸钠溶液,并进行有关实验。请回答下列问题:
(1)需称量无水碳酸钠的质量 g。
(2)配制该碳酸钠溶液时使用的仪器除天平(带砝码)、烧杯、玻璃棒外,还必须 用到的仪器有 、 等。
(3)取所配制的碳酸钠溶液125 mL,向其加入125 mL 3mol·L-1 的硫酸溶液,待充分反应后,生成的气体在标准状况下所占的体积为(假设产生的气体全部逸出) ;设反应后溶液的体积为250mL,则反应后溶液中Na+的物质的量浓度为 。
25.(5分)(1)由光导纤维组成的光缆可以代替通讯电缆,用于光纤通信,传送高强度的激光。光导纤维主要成份的化学式是 。
(2)氮化硅(Si3N4)是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业上曾普遍采用高纯硅和纯氮在1300℃时反应获得氮化硅,试写出该反应的化学方程式: ;现在主要是利用四氯化硅、氮气和氢气在强热条件下反应来获得高纯氮化硅,请写出该反应的化学方程式: 。
24.(5分)细菌的繁殖需要核酸,核酸的合成需要二氢叶酸。在二氢叶酸的合成过程中,对氨基苯甲酸是一种极其关键的物质,其结构简式为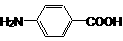 。
。
(1)它的分子式是 ;官能团-COOH的名称是 ;
(2)在它的水溶液中滴入紫色石蕊试液,溶液颜色变红,说明它的溶液具有 性;
(3)在其水溶液中加入碳酸钠溶液会产生大量气体,产生该气体的化学方程式是(用
R-COOH表示对氨基苯甲酸) ;
(4)对氨基苯甲酸可以和另一种氨基酸反应生成一种二肽(其结构为
 ),则另一种氨基酸的结构简式为 。
),则另一种氨基酸的结构简式为 。
23.下列举措不能防止或减缓钢铁腐蚀的是 ( )
A.在钢铁制品表面镀一层金属锌
B.将钢铁制品放置在潮湿处
C.在钢铁中加入锰、铬等金属,以改变钢铁结构
D.将钢铁制品与电源负极相连
22.下列纤维的主要成份是蛋白质的是 ( )
A.棉花 B.蚕丝 C.尼龙 D.人造羊毛
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com