
题目列表(包括答案和解析)
17.一定条件下.在密闭容器内,SO2氧化成SO3:2SO2 (g) + O2 (g)
 2SO3
(g) ;△H=a kJ·mol-1
在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是 A.4molSO2和2molO2
B.5molSO2和3molO2
2SO3
(g) ;△H=a kJ·mol-1
在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是 A.4molSO2和2molO2
B.5molSO2和3molO2
C.4molSO2和4molO2 D.2molSO2、1molO2和2molSO3
[ ] 18.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为
18.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为
A.5.6 g B.11.2g C.22.4g D.33.6g
16.在密闭容器中,对于可逆反应A+3B 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断不正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断不正确的是
A. 若正反应方向ΔH>0,则T1>T2
B. 压强增大时,混合气体的平均相对分子质量增大
C. A可能为气体
D. B不一定为气体
15.有一种锂电池,它是用金属锂和石墨作电极材料,电解质溶液是由LiAlCl4溶解在亚硫酰氯(SOCl2)中形成的,电池总反应为:8Li +3SOCl2===6LiCl +Li2SO3 +2S,下列有关叙述正确的是
A.金属锂作电池的正极,石墨作电池的负极
B.电池工作过程中,SOCl2被还原为Li2SO3
 C.电解质溶液中混入水,对电池反应无影响
C.电解质溶液中混入水,对电池反应无影响
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4 :1
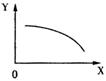
14.在一定条件下,固定容积的密闭器中反应:2NO2(g) 2NO(g)+O2(g);ΔH>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO(g)+O2(g);ΔH>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
A. 当X表示温度时,Y表示NO的物质的量
B. 当X表示压强时,Y表示NO2的转化率
C. 当X表示反应时间时,Y表示混合气体的密度
D. 当X表示NO2的物质的量时,Y表示NO的物质的量
13.下列有关铁元素的叙述中正确的是
A.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3
B.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI===FeI3+3H2O
C. 氢氧化铁可以由相关物质通过化合反应而制得
 D.铁元素位于周期表的第四周期第ⅧB族
D.铁元素位于周期表的第四周期第ⅧB族
12.某密闭容器中进行如下反应:2X(g)+Y(g) 2Z(g),若要使平衡时反应物总物质的量与生成物的物质的量相等,且用X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
2Z(g),若要使平衡时反应物总物质的量与生成物的物质的量相等,且用X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
A. 1<x/y<3 B. 1/4<x/y<2/3 C. 2/3<x/y<4 D. 1/4<x/y<3/2
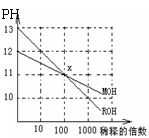
11.在25℃时将pH=11 的NaOH 溶液与pH=3 的CH3COOH溶掖等体积混合后,下列关系式中正确的是
A.c (Na+)==c(CH3COO-)+c(CH3COOH) B.c(H+)==c(CH3COO-)+c(OH一)
C.c (Na+) > c (CH3COO-)>c(OH-)>c(H+) D.c (CH3COO-)>c(Na+)>c(H+)>c(OH-)
10.在AlCl3和FeCl3混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得到的沉淀物是
A.Fe(OH)3、Al(OH)3 B.Al(OH)3、I2 C.Fe2S3、I2 D.FeS、S、Al(OH)3
9.将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是
A.Ca(OH)2的溶解度、溶剂的质量 B.溶液中溶质的质量分数
C.溶液的质量、水的电离平衡 D.溶液中Ca2+的数目、Ca(OH)2的溶解平衡
8.下列离子方程式或化学方程式中正确的是
A.氯气通入水中 Cl2 + H2O = 2H+ + Cl-+ ClO-
B.向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+ ==Fe3++3H2O
C.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3- == 3Fe3++NO↑+2H2O
D.向Mg(HCO3)2溶液中加入过量的苛性钠溶液: Mg2++2HCO3-+2OH-==MgCO3↓ +CO32-+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com