
题目列表(包括答案和解析)
12.下列事实与氢键有关的是
A.水加热到很高的温度都难以分解
B.CH4、SiH4、GeH4熔点依次升高
C.水结冰成体积膨胀,密度减少
D.HF、HCI、HBr的热稳定性依次减弱
11.下列说法中正确的是:
A.第三周期的元素中钠的第一电离能最小
B.铝的第一电离能比镁的第一电离能大
C.在所有的元素中,氟的第一电离能最大
D.在所有的元素中,氟的电负性最大
10.人们把“有相同价电子数和相同原子数的分子或离子具有相同结构特征的原理称为等电子原理”,下列各组不符合等电子原理的是
A.SiCl4 和 SO42- B.AlP 和 GaAs
C.CO2 和 N2O D.H2O2 和 H2O
9.在常温压下呈现气态的化合物,降温使其固化得到晶体属于
A.分子晶体 B.原子晶体 C.离子晶体 D.何种晶体无法判断
8.σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道或一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成.则下列分子中的σ键是由两个原子的s轨道以“头碰头”方式重叠构建而成的是
A.H2 B.HCl C.NH3 D.F2
7.元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化 B.元素原子量依次递增
C.元素的最高正化合价呈周期性变化 D.原子最外层电子排布呈周期性变化
6.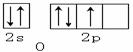
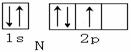 下列用轨道表示式表示原子的价电子排布正确的是
下列用轨道表示式表示原子的价电子排布正确的是
A. B.
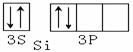
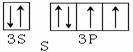 C.
D.
C.
D.
5.下列图象中所发生的现象与电子的跃迁无关的是

A.燃放焰火 B.霓虹灯广告 C.平面镜成像 D.燃烧蜡烛
4.以下各分子中,所有原子都满足最外层为8电子结构的是
A.H3O+ B.BF3
C.CCl4 D.PCl5
3.构造原理揭示的电子排布能级顺序,实质是各能级能量高低顺序。若以E表示某能级的能量,下列能量大小顺序中正确的是
A.E(3s)>E(3p)>E(3d) B.E(3s)>E(2s)>E(1s)
C. E(3d)>E(2p)>E(3s) D. E(4f)>E(4s)>E(3d)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com