
题目列表(包括答案和解析)
1、下列说法正确的是:( )
①正常雨水的pH为7.0,酸雨的pH小于7.0
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼
A.①②③ B.①④⑤ C.②③④ D.③④⑤
24.煤的气化这一重要的绿色化学技术在国外得到很大的发展,虽然在我国的研究工作刚刚起步,但是仍取得了令世人刮目相看的成果。煤的气化过程主要包括热解、气化和燃烧。主要反应[以长烟煤(C10000H8470O794)为例]:2CHxOy→2(1-y)C+2yCO+xH2
(1)上述方程式中x= ,y= ;
(2)上述反应产物中CO和H2是化工生产的原料气。现有1t长烟煤(令C10000H8470O794的式量为M、下同)按上式进行.
若煤的转化率为90%,可生成原料气 t(可以仅列出计算式、下同);
若用CO和H2在催化条件下生成C6的烷烃,这是人工合成汽油的方法之一,碳原子全部用于合成汽油,假设碳原子的利用率为a,则1t长烟煤生产烷烃 t;
23.某化学兴趣小组取1mol KMnO4样品(假设是纯净物),加热部分分解,得到a mol O2,残留固体与足量的浓盐酸充分反应,得到b molCl2,又知锰元素全部转化为 Mn2+。
(1)该小组的某同学甲未通过复杂计算判断出反应消耗的作为酸的盐酸溶质物质的量n(HCl)(不计还原剂的量)为定值,这一判断可能吗? (选填“可能”或 “不可能”),若选填不可能,则以下两格不填;若选可能,则分析甲同学判断依据是 ,且n(HCl)= mol;
(2) 该小组分析得到a、b的关系式,则关系式是 ;
且a+b的最大值为 。
22.法国化学家V.Grignard,所发明的Grignard试剂(卤代烃基镁)广泛运用于有机合成。Grignard试剂的合成方法是:RX+Mg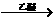 RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
RMgX(Grignard试剂)。生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
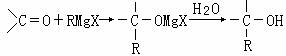
现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的具有六元环的物质J,合成线路如下,H的一氯代物只有3种。
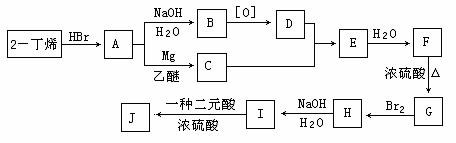
请按要求填空:
(1)F的结构简式是 ;
(2)C+D→E的反应类型是 ,F→G的反应类型是 ;
(3)写出下列化学反应方程式(有机物请用结构简式表示):
A→B ,
I→J 。
(4)I和该二元酸除了能反应生成J外,还可以在一定条件下发生缩聚反应生成高聚物,试写出此高聚物的结构简式 。
21.A、B两种有机物的结构简式如图:CH3CH(R)COOH,R表示某种官能团。A的式量是90,B的式量是89。
(1)A、B分子中不同官能团的名称分别是 和 ,均 (选填“含”或“不含”)手性碳原子;
(2)A的某种同分异构体核磁共振氢谱有一种吸收峰,则该有机物的结构简式是 ,B的某种同分异构体核磁共振氢谱有两种吸收峰,其强度比是1:6,则该有机物的结构简式是 ;
(3) A、B的两个分子之间发生反应失去一个水分子,则生成物的结构简式是
或 。
20.(1) 一定量的碳酸钠、碳酸氢钠、氢氧化钠组成的混合物,
溶解于水后溶液中的溶质成分可能是
① ,② ③ ;
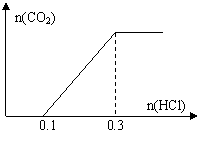
若在该溶液中加入盐酸其图像如图,则溶质的成分应是
(填①②③编号),发生的离子方程式是 ;
(2)某氧化还原反应过程中有下列物质组成:CrCl3、Cl2、
K2Cr2O7、HCl、H2O,请写出反应的化学方程式
,其中氧化剂是 ,被氧化的元素是 ,转移6mol电子时,生成的氧化产物 mol。
19.A、B、C、D、E五种短周期元素,原子序数依次增大,A、E元素在同一主族,A阳离子是一个质子,B原子最外层s、p能级电子数相等,A、D元素可形成多种化合物。
回答下列问题:
(1)E在周期表中的位置是 ,B的电子排布式是 ;
(2)以上元素可以组成多种10电子和18电子微粒。
①写出10电子阳离子的化学式: (写3种)
②写出18电子分子或离子的化学式: (写3种)
(3)以上元素可以组成多种电解质,它们水溶液有的呈现一定的酸碱性。
①溶液呈酸性,该电解质的化学式: (写3种)
②溶液呈碱性,该电解质的化学式: (写3种)
18.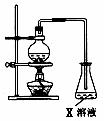 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。如图装置是乙酸乙酯的实验室和工业制法常采用如下反应:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。如图装置是乙酸乙酯的实验室和工业制法常采用如下反应:
请根据要求回答下列问题:
(1)烧瓶中主要的制备反应是 ;装置中X的化学式是 。
(2) 若用右图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为 、 等。如何提高乙酸乙酯的产率,请提出一个方案 。
(3)此反应以浓硫酸为催化剂,可能会造成 、 等问题。目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
|
同一反应时间 |
同一反应温度 |
||||
|
反应温度/℃ |
转化率(%) |
选择性(%) |
反应时间/h |
转化率(%) |
选择性(%) |
|
40 |
77.8 |
100 |
2 |
80.2 |
100 |
|
60 |
92.3 |
100 |
3 |
87.8 |
100 |
|
80 |
92.6 |
100 |
4 |
92.3 |
100 |
|
120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
|
★选择性100%表示反应生成的产物是乙酸乙酯和水 |
①根据表中数据,下列 (填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
② 当反应温度达到120℃时,反应选择性降低的原因可能为
17. (1)下列操作不正确的是(多选倒扣分)__________________
A.用渗析法分离淀粉中混有的NaCl杂质
B.用酒精清洗附着有碘晶体的试管
C.将金属钠放在煤油中保存
D.苯中溶有苯酚杂质,可向其中加入适量的浓溴水,然后过滤
E.用分液漏斗分离乙醛和水的混合物
(2)某课外活动小组证实有机物CH2=CHCHO含碳碳双键。经查阅资料得知溴水能氧化醛基,实验步骤是①取10%的NaOH溶液5mL,滴入2%CuSO4溶液6滴,振荡后加入该有机物10滴,加热,现象是 ;② 取实验①后上层溶液加入溴水,振荡溶液溴水迅速褪色。
该小组报告称达到实验目标。你的评价是:
。
16.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是
A.K+一定存在 B.100mL溶液中含0.01mol CO32-
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在
第二卷 非选择题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com