
题目列表(包括答案和解析)
5.以下原子能产生发射光谱的是
A.1s22s1 B.1s22s22p1 C. 1s22s12p2 D. 1s22s22p3
4.目前人类已发现的非金属元素除稀有气体外,共有 16 种.下列对这16种非金属元素的相关判断
①.都是主族元素,最外层电子数都大于4
②.单质在反应中都只能作氧化剂
③.氢化物常温下都是气态,所以又叫气态氢化物
④.氧化物常温下都可以与水反应生成酸
A.有①②正确 B.只有①③正确 C.只有③④正确 D.①②③④均不正确
3.元素性质呈周期性变化的决定因素是
A.元素原子半径大小呈周期性变化 B.元素原子量依次递增
C.元素原子核外电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化
2.火星探测器发回的信息表明,火星上存在针铁矿[Goethite,化学式:FeO(OH)]和黄钾铁矾[Jarosite],从而证明火星表面曾经存在过水.这一发现被《人民日报》评为2005世界十大新闻之首.已知两种矿物中铁的价态相同,则黄钾铁矾{化学式记为:KFe3(SO4)2(OH)n}中n值为
A.4 B.6 C. 5 D.7
1.科学家对原子结构的认识顺序正确的是
①.道尔顿原子模型 ②.卢瑟福原子模型 ③.汤姆生原子模型 ④.电子云模型
A.①②③④ B.④①②③ C.④②③① D.①③②④
26、(15分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
a |
|
|
|||||||||||||||
|
b |
|
|
|
c |
d |
e |
f |
|
|||||||||
|
g |
h |
i |
j |
|
k |
l |
m |
||||||||||
|
n |
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
(1)请写出元素o在元素周期表中的位置 ;
(2)d的氢化物的分子构型为 ;
(3)第三周期8种元素按单质熔点由高到低的顺序如下图,其中序号“8”代表 (填元素符号);其中非金属性最强的是 (填下图中的序号)。
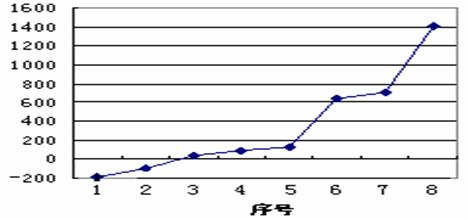
(4)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释:
。
(5)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
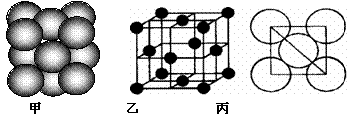
若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,则:该晶体的密度为 (用含有字母的式子表示)。
25、(10分)(2007山东卷)工业上对海水资源综合开发利用的部分工艺流程如下图所示。
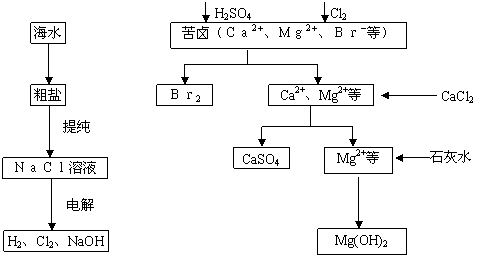
(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是 。电解槽中的阳极材料为 。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、
Mg(OH)2、CaSO4的顺序制备? ,原因是 。
(3)溴单质在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是
24、(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+ 4H++3e → NO + 2H2O
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了 、 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是 mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是: 。
23、(15分)
A、B、C、D、E均为可溶于水的固体,组成它们的离子有
|
阳离子 |
Na+
Mg2+ Al3+ Ba2+ |
|
阴离子 |
OH- Cl- CO32- SO42- HSO4- |
分别取它们的水溶液进行实验。结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。据此推断它们是
A ;B ;C ;D ;E
22.(4分)下列有关化学实验的基本操作及安全知识的叙述,
不正确的是 (填序号)。
A.用托盘天平称取10.50g干燥的NaCl固体
B.附着于试管内壁的苯酚,可用碱液洗涤
C.用碱式滴定管量取20.00mL0.1000mol/L的高锰酸钾溶液
D.用渗析法分离淀粉中混有的NaNO3杂质
E.配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌
F.切割白磷时,必须用镊子夹取,置于桌面上的玻璃片上,小心用刀切割
G.实验时,不慎打翻燃着的酒精灯,可立即用湿抹布盖灭火焰
H.用重结晶法可以除去硝酸钾中混有的少量氯化钠
I. 配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,应立即用滴管吸去多余的部分。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com