
题目列表(包括答案和解析)
31、ACV是一种由苹果发酵而成的酸性饮品,是具有明显药效的健康食品,有解毒、降脂、减肥和止泻功能。苹果酸是这种饮料的主要酸性物质,分离提纯后的化学分析如下:
①元素分析证明该酸只含C、H、O三种元素,其中C、H、O的质量比为24:3:40;该酸蒸气的密度是同温同压下氢气密度的67倍。
②0.1mol该酸与足量NaHCO3,反应放出4.48LCO2;等量的该酸与足量金属钠反应放出3.36L H2(气体体积均已折算为标准状况下的体积)。
请回答下列问题:
(1)该酸的分子式为 ;若已知该物质所有碳原子成直链状,则其结构简式为 。(2)写出该酸在加热和Cu / Ag催化条件下,被氧气氧化的反应化学方程式 。
30、.在2L密闭容器中放入a mol A﹑b mol B,在一定条件下发生如下反应:
2A(g)
+ B(g) 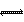 3C(g)若经过t分钟反应达平衡状态,测得前t分钟C物质的生成速度为W mol/(L﹒min),则A物质的转化率为 ,B物质的平衡浓度为
.
3C(g)若经过t分钟反应达平衡状态,测得前t分钟C物质的生成速度为W mol/(L﹒min),则A物质的转化率为 ,B物质的平衡浓度为
.
29、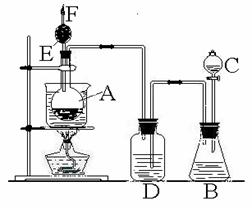 右图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图。在烧瓶A中放一些新制的无水硫酸铜粉末,并加入约20 mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓硫酸;干燥管F中填满碱石灰;烧杯作水浴器。当打开分液漏斗的活塞后,由于浓硫酸流入B中,则D中导管口有气泡产生。此时水浴加热,发生化学反应。过几分钟,无水硫酸铜粉末由无色变为蓝色,生成的气体从F顶端逸出。试回答:
右图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图。在烧瓶A中放一些新制的无水硫酸铜粉末,并加入约20 mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓硫酸;干燥管F中填满碱石灰;烧杯作水浴器。当打开分液漏斗的活塞后,由于浓硫酸流入B中,则D中导管口有气泡产生。此时水浴加热,发生化学反应。过几分钟,无水硫酸铜粉末由无色变为蓝色,生成的气体从F顶端逸出。试回答:
(1) B逸出的主要气体名称__________;
(2) D的作用是___________________;
(3) E的作用是___________________;
(4) F管口点燃的气体分子式__________________
(5) A中无水硫酸铜粉末变蓝的原因是____________________________;
(6)A中发生的方程式
28、(1)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+C02(g)+2H20(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H20(g) △H=-1160 kJ·mol-1
标准状况下4.48L CH4还原NO2至N2整个过程中放出_______ kJ热量。
(2)依据事实,写出下列反应的热化学方程式。
A.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___________________________
B.若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量_______________________________
C.用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。 ___________________________________
D.已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________
27、①CaCO3(s) == CaO + CO2(g);ΔH= 177.7kJ/mol
②C(s) + H2O(g)== CO(g) + H2(g);ΔH= -131.3kJ/mol
③0.5H2SO4(l) + NaOH(l) == 0.5Na2SO4(l) + H2O(l);ΔH= -57.3kJ/mol
④C(s) + O2(g) == CO2(g);ΔH=-393.5kJ/mol
⑤CO(g) + 1/2 O2(g) == CO2(g);ΔH=-283kJ/mol
⑥HNO3 (aq) + NaOH(aq) == NaNO3(aq) + H2O(l);ΔH= -57.3kJ/mol
⑦2H2(g) + O2(g) == 2H2O(l);ΔH= -517.6kJ/mol
(1)上述热化学方程式中,不正确的有___________
(2)根据上述信息,写出C转化为CO的热化学方程式______________________________。
(3)上述反应中,表示燃烧热的热化学方程式有_________;表示中和热的热化学方程式有______________。
26、对于A+2B(气)
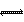 nC(气) 在一定条件下达到平衡后,改变下列条件,请回答:
nC(气) 在一定条件下达到平衡后,改变下列条件,请回答:
(1)增压,平衡不移动,当n=2时,
A的状态为 ;当n=3时,A的状态为 .
(2)若A为固态,增大压强,C的组分含量减少,则n .
(3)升温,平衡向右移动,则该反应的逆反应为 热反应.
25、2.3g某液态有机物和一定量的氧气混合点燃,恰好完全燃烧,生成2.7g水和2.24LCO2(标准状况)并放出68.35kJ热量,则该反应的热化学方程式是
24、下列有关实验的叙述,正确的是(填序号)
A、用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B、分馏石油时,温度计的末端必须插入液面下
C、用分液漏斗分离环己烷和水的混合液体
D、用浓氨水洗涤做过银镜反应的试管
E、配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
F、用酒精洗涤盛放过苯酚的试管;
G、用热NaOH溶液洗涤有油脂的试管
23、下列各组物质 ① O2和O3 ② H2、D2、T2 ③ 12C和14C ④ CH3CH2CH2CH3 和 (CH3)2CHCH3⑤乙烷和丁烷⑥CH3CH2CH2CH(C2H5)CH3 和 CH3CH2CH2CH(CH3)C2H5
互为同系物的是__________, 互为同分异构体的是_____________
互为同位素的是______, 互为同素异形体的是__________,
是同一物质的是_______。
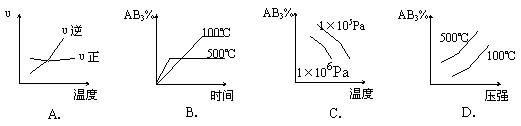
22、对于可逆反应 2AB3(g) 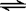 A2(g) + 3B2(g) (正反应吸热)下列图像正确的是
A2(g) + 3B2(g) (正反应吸热)下列图像正确的是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com