
题目列表(包括答案和解析)
27.(6分)在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉浮的物质的量(mol)的关系如右图所示。

(1)图中线段OA∶AB= ;
(2)若得到0.25 mol的沉淀,则加入NaOH物质的量为 。
26.( 4分)某同学猜测,铝热反应所得到的熔融物是铁铝合金。
(1)根据已有知识找出一种验证产物中有Fe的最简单方法:
;
(2)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝。(只用反应离子方程式表示): 。
25.(6分)下列框图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。已知:A是固体单质,Y是一种无色液体,既可作氧化剂,又可作还原剂,B、X均为气体单质,D属于可溶于水的强电解质,一个D分子含有18个电子。
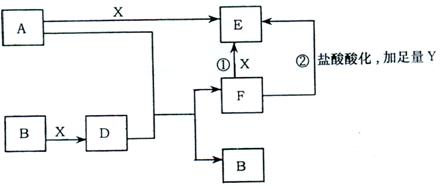
(1) A原子最外层有 个电子;
(2)写出反应①的化学方程式: ;
(3)写出反应②的离子方程式: 。
24.(6分)已知铁溶于一定浓度的硝酸溶液中反应的离子方程式为(系数a-k均为正整数):aFe+bNO3-+cH+→dFe2++fFe3++gNO↑+hN2O↑+kH2O。回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是
(用一个代数式表示,下同。):____________________________ ___
;
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是:__________________
;
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是:______________
;
23.将铝粉与某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为( )
A.11.20L B.15.68L C.22.40L D.31.36L
安溪一中08届高二(上)第二次阶段考试
化 学 试 题
第II卷(非选择题,共31分)
说明:第II卷所有答案均填在答题卡上,答在试卷上的答案均无效。
可能用到的相对原子质量:H-1 He-4 C-12 N-14 O-16 Na-23 Mg-24 A1-27 S-32 C1-35.5 K-39 Ca-40 Fe-56 Cu-64 Zn-65 Ag-108 Ba-137
22.2.1g镁铝合金完全溶于足量盐酸,生成氢气2.24L(标准状态下),再向溶液中加入氢氧化钠溶液,生成沉淀的质量最大的是( )
A.2.9g B.4.6g C.5.5g D.6.9g
21.C8H18中含4个-CH3且存在1个C原子不与H相连接的结构有( )种
A.1 B.2 C.3 D.4
20.向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.14mol B.0.16mol C.0.21mol D.0.24mol
19.实验室制备硝酸铝[AI(NO3)3·9H20]可使用下列方法:

下列说法或反映上述有关反应的离子方程式错误的是( )
A.制备过程中加HNO3应该过量,以防止蒸发时Al(NO3)3水解
B.不直接用铝片跟稀硝酸反应制硝酸铝主要是因为铝在稀硝酸中发生钝化
C.Al(OH)3沉淀不溶于NH4Cl
D.3H++Al(OH)3=A13+ +3H2O
18.蛇纹石由MgO、A12O3、Si02、Fe203组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加人NaOH溶液至过量。下列叙述不正确的是( )
A.沉淀X的成分是Si02
B.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
C.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3,
D.在溶液Y中加人过量的NaOH溶液,过滤,得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com