
题目列表(包括答案和解析)
7.在已经处于化学平衡的体系中,如果下列物理量发生变化,其中一定能表明平衡移动的是
A.反应混合物的浓度 B.反应物的转化率
C.正、逆反应速率 D.反应混合物的压强
0.6mol、 B:0.3mol 、 C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%,
则x值为
A.4 B.3 C.2 D.1
6.在一恒定的容器中充入2molA和1 mol B发生反应:2A(g)+B(g) x C(g),达到
平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:
5.在体积为VL的密闭容器中进行如下反应:mA+nB=pC+qD
用A物的浓度变化表示的平均反应速率为 ,则t min时,D物增加的物质的量是
,则t min时,D物增加的物质的量是
(A)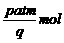 (B)
(B)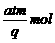 (C)
(C) (D)
(D)
4.等质量的两份锌粉a、b,分别加入过量的稀H2SO4,同时向a中加入少量的CuSO4溶液,下列图表示产生H2的体积(V)与时间(t)的关系,其中正确的是:

3.x、y均为短周期元素,且x为ⅠA族元素,y为VIA族元素。下列说法正确的是
A.x的原子半径一定大于y的原子半径
B.由x、y形成的共价化合物中所有原子都满足最外层为8电子结构
C.x2y既可能是离子化合物,也可能是共价化合物
D.由x、y组成的化合物中,x、y的原子个数比不可能是1:1
2.1999年度诺贝尔奖获得者AbmedH·ZeWapl,开创了“飞秒化学 10-15S)的新领域,使运用激光光谱技术观测化学反应时分子中原子的运动成为可能,你认为该技术不能观察到的是
A、化学变化中反应物分子的分解 B、反应中原子的运动
C、化学变化中生成物分子的形成 D、原子核的内部结构
1.痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种:
人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小心地涂到纸上,
溶液①中的溶质就跟汗渍中的物质②作用,生成物质③,物质③在光照下,分解出的银粒呈
灰褐色,随着反应的进行,银粒逐渐增多,由棕色变成黑色的指纹线。用下列化学式表示这
三种物质都正确的是 ( )
A、①AgNO3②NaBr③AgBr B、①AgNO3②NaCl③AgCl
C、①AgCl②AgNO3③NaCl D、①AgNO3②NaI③AgI
8、

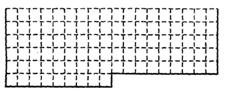
(1)上表中实线是周期表部分边界,请在表中用实线补全元素周期表边界。
(2)元素甲是第三周期第ⅥA族元素,请在右边方框中按氦元素式样写出甲的原子序数、元素符号、元素名称、相对原子质量和最外层电子排布。
(3)元素乙的3p亚层上只有1个电子,元素丙最内层电子是最外层电子的2倍,且核外p亚层电子比s亚层电子多1个,则三种元素
原子半径比较:_______>______>______(填元素符号,下同);
离子半径比较:_______>______>______;
电负性比较:_______>______>______;
第一电离能比较:_______>______>______。
(4)①用元素符号将甲、乙、丙三种元素填写在上面元素周期表中对应的位置上
②乙、丙两元素相比较,金属性较强的是________(填名称),可以验证该结论的实验是____________
a.将两种元素的块状单质分别放入水中
b.将这两种元素的单质分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别与H2反应观察反应的难易程度
d.比较这两种元素的气态氢化物的稳定性
(5)元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的________,请写出元素在周期表中的位置与元素原子结构的关系:
_____________________________________________________________________
_____________________________________________________________________
7、某些化学键的键能如下所示( )
)
|
键 |
H-H |
Br-Br |
I-I |
Cl-Cl |
H-Cl |
H-I |
H-Br |
|
键能 |
436 |
193.7 |
152.7 |
242.7 |
431.8 |
298.7 |
366 |
① 在
在 中燃烧,放出热量___________KJ
中燃烧,放出热量___________KJ
②在一定条件下, 与足量的Cl2、Br2、I2分别反应,放出热量由多到少的是_________
与足量的Cl2、Br2、I2分别反应,放出热量由多到少的是_________
A、Cl2>Br2>I2 B、I2>Br2>Cl2

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com