
题目列表(包括答案和解析)
1.化学方程式在量的方面的含义:
例如: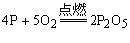
在量的方面:(1)表示反应物与生成物的质量比为124:160:284
(2)反应物总质量份数(124+160)等于生成物总质量份数(284)符合质量守恒定律
(五)板书设计
|
碳及碳的化合物 一、碳及碳的化合物的性质 二、CO2的制法 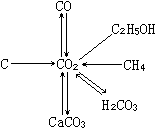 1.实验室制法 1.实验室制法2.工业制法 |
附录1-1:《碳和碳的化合物》部分典型例题
例题:
1.实验室制取CO2,常用的原料是( )
A.燃烧木炭 B.大理石与稀盐酸反应
C.石灰石与硫酸反应 D.煅烧石灰石
分析:此题考查的是二氧化碳的实验室制法,用木炭与氧气反应能生成二氧化碳,但不便于收集,故不选A,不宜用C,因为会生成微溶物CaSO4覆盖在石灰石表面阻止反应继续进行;D是工业上制取CO2的方法,所以选择B.
2.二氧化碳能灭火是由于它具有的性质是( )
A.密度比空气大 B.不能燃烧,也不支持燃烧
C.能与水反应 D.能溶于水
分析:此题的测试点为CO2的用途与性质,学生需分析CO2的性质和可燃物燃烧条件基础上分析。因为CO2密度比空气大,且不能支持燃烧,它会覆盖在可燃物上,使之与氧气隔绝,而停止燃烧,故答案为:A、B。
3.要除去一氧化碳气体中的少量二氧化碳,应将气体( )
A.通入灼热氧化铜 B.通入石灰水
C.通入水 D.点燃
分析:此题的测试点是CO、CO2的化学性质。根据它们性质的差异要除去CO2应选择B。因为CO2不能与灼热氧化铜反应,也不能燃烧所以不选择A、D;CO2微溶于水所以水不能除尽CO2,因此不能选择C。
4.长期盛放石灰水的试剂瓶壁会有一层白膜,该物质是____,要洗净该试剂瓶宜采取的方法是____。
分析:此题测试点为二氧化碳的化学性质和实验室制法,根据二氧化碳能与石灰水反应生成难溶性的碳酸钙可知白色固体为碳酸钙,根据二氧化碳的实验室制法的反应原理可知碳酸钙虽不溶于水,但溶于稀盐酸,所以此题答案为:
(1)碳酸钙 (2)加入稀盐酸溶解后,再用水洗
附录1-2《碳和碳水化合物》练习:
选择:
1.下列关于物质的用途与其所依据的性质不符合的是( )
A.金刚石用于刻划玻璃----金刚石硬度最大
B.活性炭用于冰箱除臭剂----活性炭有吸附性
C.一氧化碳用于冶炼生铁----一氧化碳有可燃性
D.干冰用于人工降雨----干冰蒸发时可吸收热量
2.下列具有可燃性、还原性、且在空气中燃烧产物相同的一组是( )
A.H2和C B.H2和CO C.CO和C D.CO和CO2
3.相同质量的碳酸钙,其中一份跟足量的盐酸反应,另一份充分煅烧,则所得二氧化碳的质量( )
A.前者多 B.后者多 C.一样多 D.无法比较
填空:
1.有O2、H2、CO、CO2、CH4五种气体,其中(1)能供给呼吸和支持燃烧的气体是____。(2)只能用排空气法收集的气体是____。(3)具有可燃性的气体是____。(4)最简单的有机物是____。
2.制取CO2与制取H2的发生装置相同的原因是____。
简答:
地球表面的大气中CO2的含量增多易产生温室效应,会对人类产生很大的影响,有人说温室效应的产生有利也有弊(1)你的观点呢?并说明原因。(2)为控制温室效应的产生应采取哪些措施(至少答两点)
(四)巩固深化:
1.学生总结本节内容,教师纠正培养学生的归纳能力
2.练习:(见附录)分层次练习,注意问题侧重知识的巩固和训练学生利用化学知识解决实际问题的能力。
3.作业:P117 1、4巩固深化本节内容,强化知识点
(三)讨论:
用化学方法区别(1)CO与CO2 (2)CO与CH4
学生分组讨论,探究方法,激发求知欲,培养开放性思维
(二)问题启发、引导,进入复习
1.教师引导启发学生:“学过哪些物质能通过化学反应生成CO2?”并引导学生。
在思考后按要求写出有关碳及含碳化合物之间相互转化的化学方程式。
学生在思考后写出化学方程式,并对比归纳总结:碳及含碳化合物的化学性质(板书)
教师在学生板书总结基础之上电脑展示,对比碳及碳的化合物的化学性质,使学生学会对比理解、记忆。
2.CO2的制法:
(1)实验室制法:
学生实验:制取一瓶CO2,并进行检验,教师指导、检查学生正确的操作方法,培养学生的实验能力。
(2)工业制法:(略)
(一)创设情境,导入复习:
教师设问:碳的单质有哪几种?我们学过含碳化合物有哪几种?
学生思考回答进入新的复习情境,激发学生的求知欲。
有关CO2的实验室制法所需实验仪器和药品。
教学重点:1.C、CO、CO2的化学性质
2.CO2的实验室制法
教学难点:碳单质及含碳化合物性质的区别与联系。
3.使学生认识事物之间是普遍联系的。
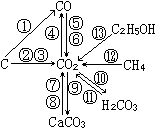 1.巩固碳及碳的几种重要化合物的性质,用途及CO2的实验室制法。
1.巩固碳及碳的几种重要化合物的性质,用途及CO2的实验室制法。
2.培养学生的归纳、对比能力。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com