
题目列表(包括答案和解析)
27.(7分)含有酚酞的氢氧化钠的溶液中,逐滴滴加新制氯水,边滴边振荡,直到红色褪去。请分析回答下列问题:
① 氯水中存在分子有:_______________和离子有:________________________。
② 氢氧化钠酚酞溶液褪色的原因可能是:
a._____________________________;b.__________________________ 。
③ 如何用实验证明你对褪色的原因的推测呢?简要叙述你的实验设计思路。
_________ _______
_________ _______ _________ _______ _______ _______ 。
26.(10分)
(1)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):
②容量瓶:
③滴定管:
④集气瓶(收集氨气):

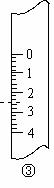
 ⑤托盘天平
⑤托盘天平
(2)右图分别是温度计、量筒、滴定管的一部分,则:
量筒应该是 ②, 读数为 mL
滴定管应该是 ,读数为 mL
温度计应该是 ,读数是 ℃
25.下列说法正确的是 AC
A.常温下醋酸分子可能存在于pH>7的碱性溶液中
B.常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中:
c(Cl-) >c(NH4 +)
C.0.1mol·L-的氯化铵溶液与0.05mol·L-的氢氧化钠溶液等体积混合后,混合溶液中离子浓度:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)
D.0.1mol·L-1硫化钠溶液中离子浓度关系: c(Na+)=c(S2-)+c(HS-)+c(H2S)
化学选修测试题
班别: 姓名: 学号: 得分:
第Ⅱ卷 非选择题(共80分)
24.取pH值均等于2的盐酸和醒酸各100ml分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是 B
A.醋酸与锌反应放出H2多B.盐酸和醋酸分别与锌反应放出的H2一样多
C.醋酸与锌反应速率小 D.盐酸和醋分别与锌反应的速度一样大
23.甲酸的下列性质中,不可以证明它是弱电解质的是 B
A.1 mol·L-1甲酸溶液的pH值约为2
B.甲酸能与水以任何比例互溶
C.10mL1 mol·L-1甲酸与10 mL1 mol·L-1NaOH溶液完全反应后,溶液呈碱性
D.在相同条件下,甲酸溶液的导电性比强酸溶液的弱
22.右图表示温度和压强对可逆反应:
2K(g)+Q(g) 2Y(g) ;△H<0的影响。
2Y(g) ;△H<0的影响。
下列有关说法可能正确的是 A
A.x轴表示Y的体积分数
B.x轴表示气体混合物的质量
C.其他条件相同时,P2下先达到化学平衡状态
D.P1<P2
21. 把Ca(OH)2放入蒸馏水中,一段时间后达到如下平衡:Ca(OH)2(s) Ca2+ (aq)+2OH-(aq)。下列说法正确的是 BC
Ca2+ (aq)+2OH-(aq)。下列说法正确的是 BC
A.加热,溶液的pH升高 B.恒温下,加入CaO,溶液pH不变
 C.加入CaCl2晶体,Ca(OH)2 固体增多 D.加入Na2CO3晶体,固体质量减少
C.加入CaCl2晶体,Ca(OH)2 固体增多 D.加入Na2CO3晶体,固体质量减少
20.在一定温度下,向饱和烧碱溶液中放入一定量的Na2O2,完全反应恢复到原温度,下列说法正确的是 CD
A.溶液中c(Na+)增大,有O2放出。 B.溶液pH值不变,有H2放出。
C.溶液中Na+数目减少,有O2放出。 D.溶液中pH值不变,有O2放出。
19.某酸HX稀溶液和某碱YOH稀溶液的物质的量浓度相等,两溶液混合后,溶液的pH大于7。下表中判断合理的是 BD
|
编号 |
HX |
YOH |
溶液的体积关系 |
|
A |
强酸 |
强碱 |
V(HX)=V(YOH) |
|
B |
强酸 |
强碱 |
V(HX)>V(YOH) |
|
C |
强酸 |
弱碱 |
V(HX)=V(YOH) |
|
D |
弱酸 |
强碱 |
V(HX)<V(YOH) |
18. Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2+ + 2H2O  Fe(OH)2 + 2H+ ,往该溶液中逐滴加入盐酸,发生的变化是 BC
Fe(OH)2 + 2H+ ,往该溶液中逐滴加入盐酸,发生的变化是 BC
A.平衡向正反应方向移动 B.平衡和逆反应方向移动
C.溶液颜色由浅绿色变为棕黄色 D.溶液由浅绿色变为灰绿色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com