
题目列表(包括答案和解析)
24.(6分)在标准状况下,有1molA气体发生如下反应:2A(g)≒B(g)+xC(g);在一定条件下反应达到平衡。在平衡混合气中,A的体积百分含量为58.6%,混合气的总质量为46g,密度为1.776g/L。求:
(1)达到平衡后混合气体的平均相对分子质量;
(2)达到平衡后A的转化率;
23.(4分)将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L,请回答:
(1)NO的体积为___________L,NO:的体积为___________L;
(2)待产生的气体全部释放后,向溶液中加入VmLamol / L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______mol / L。
 21.(10分)用如图所表示的装置、方法进行实验:
21.(10分)用如图所表示的装置、方法进行实验:
(1)实验开始一段时间后,可观察到锥形瓶口上方有白烟生成,
请将可能观察到的其他现象补齐:____________________
________________________________;有关化学方程式为
__________________________________________________
__________________________________________________
__________________________________________________;
(2)由于气温的原因,上述实验一段时间后现象不太明显,需
向锥形瓶内加入下列哪种物质才能看到明显的现象
(填代号)_______________;
A.NaOH固体 B.生石灰 C.浓H2SO4 D.NH4C1固体
(3)经过对比试验证明,在其他条件相同时,用空气代替氧气的实验效果较差,主要原因是
___________________________________________________________________________
___________________________________________________________________________。
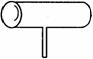 22.(9分)实验室常见到如下图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄,用该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单,操作方便,现象明显,无污染,可反复使用等优点。
22.(9分)实验室常见到如下图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄,用该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单,操作方便,现象明显,无污染,可反复使用等优点。
(1)用此仪器不能反复进行的实验是____________(填写编号)
A.NH4CI固体受热分解 B.KMnO4晶体受热分解
C.白磷和红磷互相转化 D.无水CuSO4和胆矾的互变实验
(2)当玻璃管内装有NO2和N2O4的混合气体时,亦可反复进行反应条件对化学平衡影响的实验。该实验的操作过程和实验现象是____________________________________________________
________________________________________________________________________________
________________________________________________________________________________;
(3)如果玻璃管内装有某红色溶液,加热时溶液颜色变浅,冷却时恢复红色,该溶液可能是____
__________________________;如果玻璃管内装有无色溶液,加热时溶液变缸,冷却后恢复无色,此溶液可能是____________________________________________。
20.(7分)按下图所示W是-种正盐,X、A、E都是常见气体,同温同压下A、E的密度比为2:1,
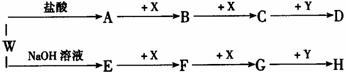 D、H是强酸。
D、H是强酸。
(1) W、X、D的化学式分别是____________、_____________、___________;
(2)W与NaOH溶液反应的离子方程式为:_________________________________;
(3)A与H稀溶液反应能生成淡黄色沉淀,此反应的化学方程式为
_____________________________________________。
19.(6分)在硫酸工业中,通过下列反应使SO2转化为SO3:2SO2+O2 2SO3+Q。已知常压下平衡混合气体SO3体积分数为91%,试回答:
(1)在生产中常用过量的空气是为了____________________________________________________
________________________________________________________________________________;
(2)加热到400℃-500℃是由于________________________________________________________
_________________________________________________________________________________;
(3)压强采用______________;原因是___________________________________________________
_________________________________________________________________________________;
(4)尾气中的SO2必须回收,原因是____________________________________________________
________________________________________________________________________________。
 17.(7分)红磷虽较稳定,但在未密闭的情况下久置往往表面发粘发潮。磷在空气中与O2作用有A生成,A的立体结构如下图A(短线代表共价键),它是白色固体,熔点23.8℃。
17.(7分)红磷虽较稳定,但在未密闭的情况下久置往往表面发粘发潮。磷在空气中与O2作用有A生成,A的立体结构如下图A(短线代表共价键),它是白色固体,熔点23.8℃。
(1)磷在空气中与O2作用生成A的化学方程式为____________________________________;
(2)A在空气中受热可转化为B,B的立体结构如图B,它的化学式为_____________;
写出B与热水反应的化学方程式______________________________________;
(3)写出A与HCl气体反应生成能在空气中形成白雾的气体的化学方程式
__________________________________________。
18.(3分)近些年来,某些自来水厂在用液氯进行消毒处理时还加入少量液氨,其反应的化学方程式:NH3+HClO≒H2O+NH2Cl(一氯氨),NH2C1较HClO稳定,试分析加液氨能延长液氯杀菌时间的原因_________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________。

16.-个真空密闭容器中盛有lmolPCl5,加热到加200℃时发生了反应PCl5(g)≒PCl3(g)+Cl2(g),反应达到平衡后PCl5的转化率为M%,若在同一温度下和同样容器中最初投入的是2molPCl5,反应达到平衡时PCl5的转化率为N%,M与N的关系正确的是
A.M>N B.M<N C.M=N D.不能确定
15.为了除去铝表面的铜镀层可选用的试剂是
A.稀HNO3 B.浓HNO3 C.浓H2SO4 D.浓盐酸
13.下列离子方程式书写正确的是
A.氯化铵溶液与氢氧化钠稀溶液混合:NH4++OH-=NH3↑+H2O
B.稀HNO3和Cu反应:Cu+4H++NO3-=Cu2++NO2↑+2H2O
C.硝酸和氧化铜反应:2H++2NO3-+CuO=Cu(NO3)2+H2O
D.氨气与盐酸反应:NH3+H+=NH4+
 14.可逆反应mA(g)≒nB(g)+pC(s)+Q,温度和压强的变化对正逆反应速率的影响分别符合图中的两个图像,以下叙述正确的是
14.可逆反应mA(g)≒nB(g)+pC(s)+Q,温度和压强的变化对正逆反应速率的影响分别符合图中的两个图像,以下叙述正确的是
A.m>n,正反应放热
B.m>n+p,正反应放热
C.m>n,正反应吸热
D.m<n+p,正反应吸热
12.在一固定容积的密闭容器中加入2molA和lmolB发生下列反应并且达到化学平衡状态,
2A(g)+B(g)≒3C(g)+D(g)。平衡时C的浓度为a mol/L,若维持容器体积和温度不变,按下列四种配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为a mol/L的是
A.4molA+2mol B B.2molA+lmol B+3mol C+lmol D
C.3mol C+lmol D D.3mol C+lmol D+lmol B+lmol A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com