
题目列表(包括答案和解析)
16、中和10mL 1.0mol/L盐酸需消耗等体积的氢氧化钠溶液或氨水。则氢氧化钠溶液和氨水的
A.pH相同 B.电离程度相同
C.物质的量浓度相同 D.溶质的质量相同。
15、常温下,将pH=2的酸溶液和pH=12的苛性钠溶液等体积混合后,则溶液中
A.pH=7 B.pH≥7 C.pH≤7 D.[H+][OH-]=10-14
14、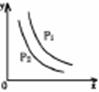 反应:L(s)+ aG(g)
反应:L(s)+ aG(g)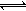 bR(g)达到平衡,温度和压强对该反应的影响如右图所示,图中:压强 P1> P2,x轴表示温度,y轴表示平衡混合气中 G 的体积分数。据此可判断
bR(g)达到平衡,温度和压强对该反应的影响如右图所示,图中:压强 P1> P2,x轴表示温度,y轴表示平衡混合气中 G 的体积分数。据此可判断
A.上述反应是放热反应 B.上述反应是吸热反应
C.a> b D.a< b
13、在同体积pH=3的硫酸,盐酸,硝酸,醋酸溶液中,加入足量的镁粉,下列说法中正确的是
A.硫酸中放出的氢气量最多 B.醋酸中放出氢气的量最多。
C.盐酸和硝酸中放出的氢气量相等 D.盐酸比硝酸放出的氢气量多。
12、在100mL 0.1mol/LCH3COOH溶液中,欲使CH3COOH电离度和溶液的pH都增大,可以采用的方法是
A.加少量1 mol/L氢氧化钠溶液 B.加少量1 mol/L盐酸
C.加100mL水 D.加热
11、某温度下,重水D2O的离子积为1.6×10-15,可以用pH一样的定义来规定pD=-lg[D+],以下关于pD的叙述正确的是
A.中性溶液中pD=7
B.在1L D2O的溶液中溶解0.01mol NaOD(设溶液体积为1L),其中pD=12
C.在1L D2O中溶解0.01mol DCl(设溶液的体积为1L),其中pD=2
D.向100mL 0.25mol·L-1的DCl重水溶液中加入50mL 0.2mol·L-1的NaOD的重水溶液,其中pD=2
10、在同温同压下,下列各组热化学方程式中,△H2>△H1的是
A.2H2(气)+O2(气)=2H2O(气) △H1
2H2(气)+O2(气)=2H2O(液) △H2 B.S(气)+O2(气)=SO2(气) △H1 S(固)+O2(气)=SO2(气) △H2 C. C(固)+1/2O2(气)=CO(气) △H1 C(固)+O2(气)=CO2(气) △H2 D.H2(气)+Cl2(气)=2HCl(气) △H1
1/2H2(气)+1/2Cl2(气)=HCl(气) △H2
9、下列电离方程式正确的是
A、醋酸溶于水:CH3COOH =CH3COO- + H+
B、熔融状态下的NaHSO4:NaHSO4 = Na+ + H+ +SO42-
C、碳酸氢钠溶于水:HCO3-
+H2O  CO32- + H3O+
CO32- + H3O+
D、硫化氢溶于水:H2S
 2H+
+ S2-
2H+
+ S2-
8、 将等体积的未知浓度的氢氧化钡溶液与0.10mol/L的盐酸混合,所得溶液的pH为12.0,则氢氧化钡溶液的物质的量浓度是
A.0.03 mol/L B.0.3mol/L C.0.06mol/L D.0.12mol/L
7、在一个固定容积的密闭容器中充入2mol NO2,一定温度下建立如下平衡:2NO2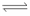 N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是
N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是
A.x>y B.x<y C.x=y D.不能确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com