
题目列表(包括答案和解析)
22].(8分)取一铝制易拉罐,取其铝片,擦去其表面的氧化物,之后将铝片剪成树状,并塞入事先洗净的雪碧塑料瓶中。取胆矾约25-30g加入雪碧瓶,之后注水,以没过树状铝片为宜,再拧紧瓶塞。装置如右图。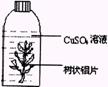
实验现象:开始在铝片表面覆盖一层紫红色物质,之后该物质越来越多,最后成绒毛状,形成美丽的“铜树”。同时发现从铝片表面产生气泡,而且产生的气体的速率越来越快。将该瓶靠近耳边,会听到“滋滋”作响,并有热感。反应一段时间后,点一根火柴,在火焰附近拧松瓶盖,会听到“嘭”的一声爆鸣。
(1)在看到产生气体的过程中,还可观察到什么实验现象?
(2)请对上述实验做出合理的解释,并写出必要的反应方程式。
21].(13分)现有含CaO杂质的CaC2试样。某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度。请填写下列空白:
(1)第一种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度。
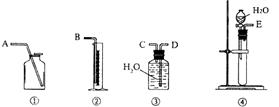
①所选用装置的连接顺序应是(填各接口的字母): 。
②若实验时称取的试样为1.40g,产生的乙炔在标准状况下的体积为448mL(1atm,25℃,此时水的饱和蒸汽(分)压为0.03atm),此试样中CaC2的质量分数为 。
|
|
读数次数 |
质量/g |
|
锥形瓶
+
水
+
试样 |
第1次 |
196.30 |
|
第2次 |
196.15 |
|
|
第3次 |
196.05 |
|
|
第4次 |
196.00 |
|
|
第5次 |
196.00 |
(2)第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数。先称取试样1.50g、锥形瓶和水的质量为195.00g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如右表:
计算CaC2的质量分数时,必需用的数据是 。不必作第6次读数的原因是 。此试样中CaC2的质量分数为 。
(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:

①操作Ⅱ的名称是 。
②还需直接测定的物理量是 。
③在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果 (填“偏大”、“偏小”或“不变”)。
④请指出该实验方案的2个不足之处
⑤请改进这个实验方案,至少解决其中1个不足之处
20].往一体积不变的密闭容器中充入一种气态烃和O2的混合气体,其体积比为1︰10,将该混合气体点火引爆,完全反应后在127℃时测得气体压强为p,恢复到常温27℃时测得气体压强为p/2,则该气态烃可能是
A CH4 B C2H6 C C4H8 D C6H10
19].有一定质量的KNO3样品,在10℃下加蒸馏水使之充分溶解,残留固体的质量为250g。该实验在40℃下进行时,残留固体质量为120g,70℃时为20g。已知KNO3在不同温度下的溶解度:
|
温度 |
10℃ |
40℃ |
55℃ |
70℃ |
|
溶解度 |
20g |
65g |
100g |
140g |
下列对该样品的推断正确的是
A 样品为纯净物 B 样品中混有不溶于水的杂质
C 样品中混有溶解度较大的杂质 D 当温度在55℃左右时KNO3完全溶解
|
一 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
二 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
|
18].对于白磷引起的中毒,硫酸铜溶液是一种解毒剂,有关反应如下:P+CuSO4+H2O-Cu3P+H3PO4+H2SO4。下列关于该反应的说法正确的是
A 白磷为还原剂、CuSO4为氧化剂 B 生成1mol H3PO4时,有5mol电子转移
C 有8/11的白磷发生了歧化反应 D 氧化产物和还原产物的物质的量之比为5︰6
17].下列说法中正确的是
A 向0.1mol·L-1 KNO3溶液中滴加稀盐酸使溶液的pH=5,此时混合液中c(K+)=c(NO3-)
B 25℃时,0.1 mol·L-1氨水和0.05 mol·L-1氨水中c(OH-)之比是2∶1
C 0.1 mol·L-1NH4Cl溶液中c(Cl-)=c(NH4+)
D 向CH3COONa溶液中加入适量CH3COOH使混合液pH=7,此时溶液中c(Na+)=c(CH3COO-)
高二化学竞赛联考题(七)
(时间:120分钟 满分:150分)
班级: 姓名:
|
H 1.008 |
相对原子质量 |
He 4.003 |
|||||||||||||||
|
Li 6.941 |
Be 9.012 |
|
B 10.81 |
C 12.01 |
N 14.01 |
O 16.00 |
F 19.00 |
Ne 20.18 |
|||||||||
|
Na 22.99 |
Mg 24.31 |
Al 26.98 |
Si 28.09 |
P 30.97 |
S 32.07 |
Cl 35.45 |
Ar 39.95 |
||||||||||
|
K 39.10 |
Ca 40.08 |
Sc 44.96 |
Ti 47.88 |
V 50.94 |
Cr 52.00 |
Mn 54.94 |
Fe 55.85 |
Co 58.93 |
Ni 58.69 |
Cu 63.55 |
Zn 65.39 |
Ga 69.72 |
Ge 72.61 |
As 74.92 |
Se 78.96 |
Br 79.90 |
Kr 83.80 |
|
Rb 85.47 |
Sr 87.62 |
Y 88.91 |
Zr 91.22 |
Nb 92.91 |
Mo 95.94 |
Tc [98] |
Ru 101.1 |
Rh 102.9 |
Pd 106.4 |
Ag 107.9 |
Cd 112.4 |
In 114.8 |
Sn 118.7 |
Sb 121.8 |
Te 127.6 |
I 126.9 |
Xe 131.3 |
|
Cs 132.9 |
Ba 137.3 |
La-Lu |
Hf 178.5 |
Ta 180.9 |
W 183.8 |
Re 186.2 |
Os 190.2 |
Ir 192.2 |
Pt 195.1 |
Au 197.0 |
Hg 200.6 |
Tl 204.4 |
Pb 207.2 |
Bi 209.0 |
Po [210] |
At [210] |
Rn [222] |
|
Fr [223] |
Ra [226] |
Ac-La |
Rf |
Db |
Sg |
Bh |
Hs |
Mt |
Ds |
|
16].现有下列短周期元素性质的数据:
|
|
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径 |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
下列说法正确的是
A 原子序数④元素大⑦元素 B ⑧号元素原子结构示意图为: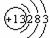
C ②、③处于同一周期 D 上述八种元素最高价氧化物对应的水化物,⑤号酸性最强
15].下列物质间反应的离子方程式错误的是
A 氧化三铁溶于氢碘酸溶液中:Fe3O4+8H++2I-=3Fe2++I2+4H2O
B 同物质的量浓度的FeI2溶液与Br2水溶液等体积混合:2I-+Br2=I2+2Br-
C 向Ba(OH)2溶液中加入过量的NH4HSO4溶液:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O
D 澄清石灰水中加入盐酸溶液:H++OH-=H2O
14].在一密闭容器中,反应mA(g)+nB(g)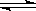 3C(g)达到平衡时,测得c(A)为0.5mol/L在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.25 mol/L。下列判断中正确的是
3C(g)达到平衡时,测得c(A)为0.5mol/L在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)为0.25 mol/L。下列判断中正确的是
A A的质量分数增加 B 平衡时逆反应速率减小
C 化学计量数:m+n=3 D 物质C的体积分数
13].下列实验操作错误的是
A 向一支洁净的试管中加入1mL 2%硝酸银溶液,再向试管中滴加2%的稀氨水至最初产生的沉淀恰好溶解为止。再滴加3滴乙醛溶液,振荡后热水浴中温热,片刻后试管内壁形成银镜
B 实验室制取乙烯时,必须将温度计的水银球插入反应液中,但不接触瓶底
C 取2mL 10%NaOH溶液于试管中,加入4mL 2%CuSO4溶液,振荡后再加入某种有机试剂,热水浴中温热,可根据是否产生红色沉淀判断该有机物中是否含有醛基。
D 取20mL蒸馏水于50mL烧杯中,加热至沸,向沸水中滴加1mL-2mL FeCl3饱和溶液,持续加热片刻,即可制得Fe(OH)3胶体。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com