
题目列表(包括答案和解析)
4.据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是
A.Fe -2e-=Fe2+ B.2H2O+O2+4e-=4OH-
C.2H++2e-=H2↑ D.4OH-- 4e-=2H2O+O2↑
3.在配置Fe2(SO4)3溶液时,为了防止水解,常常往溶液中加入少量的
A.NaOH B.H2SO4 C.KCl D.CH3COOH
2.已知在1×105Pa、298K条件下,2mol氢气燃烧生成水放出484kJ热量,下列热化学方程式正确的是
A.H2O(g)==H2(g)+ O2(g);
O2(g);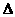 H=
+242kJ·mol-1
H=
+242kJ·mol-1
B.2H2(g)+O2(g)==2H2O(l);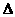 H= -484kJ·mol-1
H= -484kJ·mol-1
C.H2(g)+ O2(g)==H2O(g);
O2(g)==H2O(g);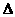 H=
+242kJ·mol-1
H=
+242kJ·mol-1
D.2H2(g)+O2(g)==2H2O(g);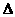 H=
-484kJ·mol-1
H=
-484kJ·mol-1
1.已知反应X+Y= M+N为放热反应,,对该反应的下列说法中正确的
A.X的能量一定高于M
B.Y的能量一定高于N
C.X和Y的总能量一定高于M和N的总能量
D.因该反应为放热反应,故不必加热就可发生
29.请在以下(1)、(2)两小题中任选一题作答,若两道题都做,则以第一道题为准。(5分) (1)为测定一种复合氧化物型的磁性粉末材料的组成,称取6.26g样品,将其全部溶于过量稀硝酸后,配成100mL溶液。取50mL溶液,加入硫酸钾溶液,生成白色沉淀,经过过滤、洗涤、烘干后得2.33g固体。另取25mL溶液,加入少量硫氰化钾溶液,显红色。再取余下的25mL溶液,加入过量氢氧化钠溶液,生成红褐色沉淀,将沉淀过滤、洗涤、灼烧后得0.80g固体。请计算并结合推理,填写下表: 组成该磁性材料元素是 各元素的质量比是 m(x) : : = : : 各元素的原子个数比是 n(x) : : = : : 该磁性材料的化学式 用氧化物的形式表示 (2)400℃,1.01×105Pa时,1.5L某烃蒸气能在aL氧气中完全燃烧,体积增大至(a+3)L(400℃,1.01×105Pa测定)请回答: ①该烃在组成上必须满足的条件是 。 ②当a=10L时,该烃可能的化学式为 (最少写出三种) ③当该烃的化学式为C7H8时,a的取值范围是 。
28.(5分)0.05mol某烃完全燃烧,生成二氧化碳气体5.6L(标准状况下)和5.4g水。
(1)通过计算写出该烃的分子式。
(2)若该烃的一氯代物只有一种结构,写出该烃的结构简式,并用系统命名法命名。
27.(10分)实验室制取乙烯的装置如下图④,试回答:
(1)烧瓶中加入的两种试剂是 ;
(2)烧瓶中发生的化学反应其化学方程式是 。
(3)实验室制乙烯时,常因温度过高而发生副反应,请写出生成二氧化硫、二氧化碳和水蒸气的化学方程式 。
(4)请用下图中编号为①-④的实验装置,设计一个实验,以验证上述反应的混合气体中含有的地氧化硫、二氧化碳和水蒸气。
用装置的编号表示装置的连接顺序(按气体从左向右的流向): → → → 。
(5)实验时装置①中A瓶中的现象是 ;结论是 ;B瓶的作用是 ;若C瓶中品红溶液不褪色,可得出的结论是 。
(6)装置③中加入的固体药品是 ;装置②中盛放的溶液是 。
26.(6分)除去下列物质中的杂质,请将所用试剂和分离操作的名称填入下表(括号中物质为杂质) 被提纯的物质 除杂所用的最佳试剂 分离操作名称
1 溴苯 (Br2)
2 C2H2 (H2S)
4 SiO2 (Al2O3)
25.(2分)有 种铁的氧化物样品Wg,加入140 mL 5 mol/L 的盐酸恰好完全溶解,假设溶解过程中Fe2+没有被空气扩大化 成Fe3+,所得溶液还能吸收0.56L(标准状况下)氯气,恰好完全反应使其中的Fe2+全部转化为Fe3+。该样品的化学式为 。
24.(7分)提示:某些金属氧货物 跟熔融烧碱反应可生成盐。根据如图所示化学反应框图进行填空。
(1)单质B是 ;单质F是 。(写化学式)
(2)写出由E生成G化学反应的离子方程式和化学方程式 ;
(3)溶液I中所含金属离子是 ;
(4)写出由I到J发生化学反应的离子方程式 ;
(5)若由C→E+F改变用浓酸,则不能选用的浓酸是(写化学式) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com