
题目列表(包括答案和解析)
27.考生注意:23题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。
A(6分)某含氧有机化合物可以作为无铅汽油的抗爆震剂,它的分子量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,红外光谱显示该分子中只有C--H和C--O键的红外吸收峰,核磁共振氢谱该显示该分子中有两种类型氢原子的吸收峰。
(1) 该有机物的的分子式为
(2)该有机物 (能或不能)与金属钠反应
(3)请写出其结构简式: 。
B(1)下列结构中,·代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,

根据各图表示的结构特点,写出该分子的化学式:
A: B:
C: D:
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用®表示,例如:

写出三硝酸甘油酯的的结构式:
。
24我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5 mol甲烷与0.5 mol水蒸汽在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是: 。
(2)在合成氨的实际生产过程中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来,并将分离出氨后的氮气和氢气循环利用,同时补充氮气和氢气。请运用化学反应速率和化学平衡的观点说明采取该措施的理由: 。
(3)当甲烷合成氨气的转化率为75%时,以5.60×107 L甲烷为原料能够合成 L氨气。(假设体积均在标准状况下测定)
(4)已知尿素的结构简式为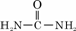 ,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
,请写出两种含有碳氧双键的尿素的同分异构体的结构简式:
① ;② 。
 25.在某一容积为2L的密闭容器内,加入0.8mol的
25.在某一容积为2L的密闭容器内,加入0.8mol的
H2和0.6mol的I2,在一定的条件下发生如下反应:
 H2(g) + I2(g)
⇌ 2HI(g) + Q (Q>0)
H2(g) + I2(g)
⇌ 2HI(g) + Q (Q>0)
反应中各物质的浓度随时间变化情况如图1:
(1)该反应的化学平衡常数表达式为
。
(2)根据图1数据,反应开始至达到平衡时,
平均速率v(HI)为
。
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K
(填写增大、减小或不变)
HI浓度的变化正确
(用图2中a-c的编号回答)
②若加入I2,H2浓度的变化正确的是
,(用图2中d-f的编号回答)
(4)反应达到平衡后,第8分钟时,若反容器
的容积扩大一倍,请在图3中画出8分钟
后HI浓度的变化情况。
26. (10分)稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2。不同空/燃比时汽车尾气中主要污染物的含量变化如右图所示。
(10分)稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2。不同空/燃比时汽车尾气中主要污染物的含量变化如右图所示。
⑴稀薄燃烧技术除能节约能源外,还具有的优点是_______________(填一项)。排放到大气中的NOx会导致酸雨、_______________等环境问题(填一项)。
⑵某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。
|
|
-→ |
催化反应器 |
-→ |
检 测 |
-→ |
尾气处理 |
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通过滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是 。
⑶若某一催化剂能同时催化NH3等还原性气体与的反应NOx的反应。将该催化剂分别用于催化还原含等物质的量NOx的两种气体:①纯NO气体,②汽车尾气。消耗的物质的量较多的可能是 (填字母),原因是 。
A.① B.② C.都有可能
22.(10分)请按要求填空:某化学课外小组用右图装置制取溴苯。
先向分液漏斗中加入苯和液溴 ,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1) 写出A中反应的化学方程式
(2) 观察到A中的现象是 。
(3) 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
(4) C中盛放CCl4的作用是 。
(5) 能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是 。
23(10分)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:

(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是
(3)实验中加热试管的目的是:
①
②
(4) 试管b中加有饱和Na2CO3溶液 ,其作用是
(5)反应结束后,振荡试管b静置,观察到的现象是
21.(10分)(1)下列实验操作或对实验事实的叙述正确的是 (填序号)
①用稀HNO3清洗做过银镜反应实验的试管;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③使淀粉在稀氢氧化钠溶液中水解可得到葡萄糖
④用托盘天平称取10.50 g干燥的NaCl固体;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧用浓硫酸和无水乙醇在140℃条件下制乙烯。
 (2)用下图装置制取和收集某种干燥的气体。
(2)用下图装置制取和收集某种干燥的气体。
(1)根据装置图填写下面的表格(填有关的化学式)
|
A内的固体化合物 |
B内的溶液 |
集气瓶中的气体 |
|
|
|
|
(2)请你归纳出能用上述装置制取的气体的特点:反应是利用固体和液体在常温下进行反应,_________________________________________。
_________________________________________。

20.某芳香族有机物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中不可能有
A.两个羟基 B.一个醛基 C.两个醛基 D.一个羧基
第II卷(非选择题,共83分)
19.某500mL溶液中含0.1molFe2+、0.2molFe3+,加入0.2mol铁粉,待Fe3+完全还原后,溶液中Fe2+的物质的量浓度为(假设反应前后体积不变)
A、0.4mol/L B、0.6mol/L C、0.8mol/L D、1.0mol/L
17.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

下列描述正确的是
A. 反应开始到10 s,用Z表示的反应速率为0.158 mol/(L·s)
B. 反应开始到10 s,X的物质的量浓度减少了0.79 mol/L
C. 反应开始到10 s时,Y的转化率为79.0%
D. 反应的化学方程式为:X(g)+Y(g)=Z(g)
18已知反应mX(g)+nY(g) qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的m/n倍
C.降低温度,混合气体的平均相对分子质量变小
D.增加X的物质的量,Y的转化率降低
16.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是
A、CH4和C3H4 B、 C3H4和C3H6
C、C2H4和C2H6 D、C2H2和C2H6
15、苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如右图。关于苏丹红说法错误的是
A、分子中含一个苯环和一个萘环
B、属于芳香烃
C、能被酸性高锰酸钾溶液氧化
D、不能溶于苯
14.下列各化合物中,使发生酯化、还原、加成、消去四种反应的是
A.CH2- -CH2-CHO B.CH2-
-CH2-CHO B.CH2- -
- -CH3
-CH3
C.CH3-CH=CH-CHO D.HOCH2- -CH2-CHO
-CH2-CHO

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com