
题目列表(包括答案和解析)
28.在一固定容器的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(气)+2B(气) 3C(气)。已知加入1 mol A和3 mol B且达到平衡后,生成了a mol C。
3C(气)。已知加入1 mol A和3 mol B且达到平衡后,生成了a mol C。
(1)达到平衡时,C在反应混合气体中的体积分数(物质的量的百分数)是 (用含a的代数式表示)。(2分)
(2) 在相同实验条件下,若在同一容器中改为加入2 mol A和6 mol B,达到平衡后,C的物质的量为 mol(用含a的代数式表示),此时C在反应混合气体中的体积分数 (填“增大”“减小”或“不变”)。(2分)
(3) 在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要求平衡后C在反应混合气体中体积分数不变,则还应加入C mol。(2分)
27.今有a、CH3COOH、b、HCl、c、H2SO4三种溶液(以下物理量均分别以a、b、c表示,有倍数关系的请标出,无倍数关系的,请标出大小关系)(共8分,每空2分)
(1)当它们的pH相同时,其物质的量浓度的关系是 。
(2)当它们的物质的量浓度相同时,其pH关系是 。
(3)中和同一烧碱溶液,需同浓度的三种溶液的体积关系是 。
(4)体积、浓度都相同的a、b、c三溶液,分别与同浓度的NaOH溶液反应,使pH等于7,所需NaOH溶液的体积关系是 。
26.(1)0.02mol/L的HCN溶液与0.02mol/L NaCN溶液等体积混合,已知该混合溶液中,
c(Na+)>c(CN-)用“>、<、=”符号填空,已知HCN是弱酸。(共8分,每空1分)
① 溶液中c(OH-)__ _c(H+) ②c(HCN)__ __c(CN-) ③c(HCN)+c(CN-)____0.02mol/L
(2).已知浓度均为0.1mol/L的8种溶液:①HNO3 ②H2SO4 ③CH3COOH ④Ba(OH)2 ⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl其溶液pH由小到大的顺序是______________________ (用序号填写)。
(3)①向明矾溶液中逐滴滴入氢氧化钡溶液至硫酸根离子刚好沉淀完全时,溶液的pH______7(填>、<、=),反应总离子方程式为___________________________;
②向明矾溶液中逐滴加氢氧化钡溶液至铝离子刚好沉淀完全时,溶液的pH______7(填>、<、=),反应总离子方程式为_____________________________。
25. 在密闭容器中一定量混合气体发生反应:2 A(g)+2B(g) xC(g),达到平衡时测得A的
在密闭容器中一定量混合气体发生反应:2 A(g)+2B(g) xC(g),达到平衡时测得A的
浓度为0.5mol/L,在温度不变的条件下,将容器中的容积扩大到原来2倍,再达平衡时, 测得A的浓度为0.3mol/L,下列有关判断正确的是 ( )
A.x=3 B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数增大
24. 在一密闭器中,等物质的量的A和B发生如下反应:A(g)+2B(g) 2C(g),一段时间后反应达到平衡,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率是 ( )
在一密闭器中,等物质的量的A和B发生如下反应:A(g)+2B(g) 2C(g),一段时间后反应达到平衡,若混合气体中A和B的物质的量之和与C的物质的量相等,则这时A的转化率是 ( )
A.40% B.50% C.60% D.70%
23.把 放入一定量的蒸馏水中,一定温度下达到平衡:
放入一定量的蒸馏水中,一定温度下达到平衡:

 .当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
.当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
A.C(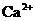 )增大 B.溶液中
)增大 B.溶液中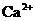 数增加
数增加
C.溶液pH增大 D.溶液pH不变
22.将适量的铁粉放入氯化铁溶液中,完全反应后,溶液中的Fe3+离子和Fe2+离子浓度相等.则已反应的Fe3+离子和未反应的Fe3+离子的物质的量之比 ( )
A.2:3 B.3:2 C.1:2 D.1:1
21.能使铁溶解,又不生成固体和气体的是 ( )
①稀H2SO4 ②稀HNO3 ③Fe2(SO4)3溶液 ④CuSO4溶液 ⑤浓H2SO4 ⑥氨水
A.②③ B.④⑤ C.①④⑥ D.③
20. 由铜、锌和稀硫酸组成的原电池工作时,电解质溶液的pH如何变化 ( )
A.不变 B.先变小后变大 C.逐渐变大 D.逐渐变小
19.将AlCl3溶液和NaAlO2溶液分别蒸干并灼烧,所得产物主要成分为
A.都是Al(OH)3 B.前者是Al2O3,后者是NaAlO2
C.都是Al2O3 D.前者是AlCl3,后者是NaAlO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com