
题目列表(包括答案和解析)
26.(12分)(1)如果反应物所具有的总能量大于生成物所具有的总能量,反应物转化为生成物时_______热量,△H 0;
(2)写出下列物质在水中电离的方程式:
①亚硫酸 , ;
②氢氧化铁___________________________________;
③碳酸氢钾__________________________________________。
25.阿伏伽德罗常数约为6.02×1023mol-1,下列说法中一定正确的是
A.1.0L1.0mol·L-1CH3COOH溶液中,CH3COOH分子数为6.02×1023
B.Na2O2与H2O反应生成11.2LO2(标准状况),反应中转移的电子数为2×6.02×1023
 C.32gS8单质中含有6.02×1023个硫原子
C.32gS8单质中含有6.02×1023个硫原子
D.22.4LN2中所含的分子个数为6.02×1023
24.在25℃、101kPa下,0.1mol甲醇燃烧生成CO2和液态水时放热72.58kJ,下列热化学方程式正确的是( )
A、CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O(l);△H=+725.8kJ/mol
B、2CH3OH(l) +3O2(g) = 2CO2(g) + 4H2O(g);△H=-1451.6kJ/mol
C、CH3OH(l) + 3/2O2(g) = CO2(g) + 2H2O(l);△H=-725.8kJ/mol
D、2CH3OH(l) + 3O2(g) = 2 CO2(g) + 4H2O(l);△H=-1451.6kJ/mol
23.
 反应2X(g)+Y(g) 2Z △H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示。则下列叙述正确的是
反应2X(g)+Y(g) 2Z △H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示。则下列叙述正确的是
A. T1>T2,P1<P2 B. T1>T2,P1>P2
C. T1<T2,P1>P2 D. T1<T2,P1<P2
22.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( ).
A.S(g) + O2(g) =SO2(g); △H1 S(s) + O2(g) = SO2(g);△H2
B.2H2(g) + O2(g)= 2H2O(g);△H1 2H2(g) + O2(g) = 2H2O(l);△H2
C.CO(g) + 1/2 O2(g) = CO2(g);△H1 2CO(g) + O2(g) = 2CO2(g);△H2
D.H2(g) +Cl2(g)=2HCl(g);△H1 1/2 H2(g) + 1/2 Cl2(g) = HCl(g);△H2
21.已知某可逆反应在密闭容器中进行:
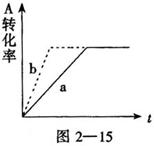
 A(g)+2B(g) C(g)+D(s)(正反应是放热反应),图2-15中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是(
)
A(g)+2B(g) C(g)+D(s)(正反应是放热反应),图2-15中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可采取的措施是(
)
A.增大A的浓度
B.缩小容器的容积
C.加入催化剂
D.升高温度
20.pH值相等的盐酸(甲)和醋酸(乙),分别与等质量的锌片反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是( )
A.反应开始时的速率:甲=乙 B.反应所需时间:甲<乙
C.反应开始时,酸的物质的量浓度:甲<乙 D.反应结束时,pH值:甲<乙
19.在一定条件下发生下列反应,其中属于盐类水解反应的是 ( )
A.NH4+ +2H2O  NH3·H2O + H3O+
NH3·H2O + H3O+
B.HCO3- + H2O  H3O+ + CO32-
H3O+ + CO32-
C.HS-+H3O+=== H2S↑+H2O D.Cl2+H2O  H++Cl-+HClO
H++Cl-+HClO
18.已知反应3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O,将铜片浸入热的稀硝酸中,片刻取出残留的铜片,发现铜片质量减少了a克,同时生成A L气体(标准状况),则被还原的硝酸的物质的量为( )
A. mol
B.
mol
B. mol C.
mol C.
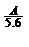 mol D.
mol D.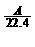 mol
mol
17.下列反应的离子方程式书写正确的是:
A. 氯化铝溶液中加入过量氨水:Al3+
+ 4NH3•H2O
AlO2- + 4NH4+
+ 2H2O
B. 澄清石灰水与少量小苏打溶液混合:Ca2+ + OH-
+ HCO3- CaCO3↓ + H2O
C. 碳酸钙溶于醋酸CaCO3
+ 2H+ Ca2+ + CO2↑ + H2O
D. 氯化亚铁溶液中通入氯气:2Fe2+
+ Cl2 2Fe3+ + 2Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com