
题目列表(包括答案和解析)
8.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A、1mol聚乙烯含有的原子数目为6NA
B、标况下1L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA /22.4
C、1mol甲基含9 NA个电子
D、0.1mol甘油与足量的钠反应,可生成标况下的氢气6.72L
7.分子式为C5H12O的醇,其分子结构中有一个碳原子不跟氢原子直接相连,则该醇的分子结构可能有 ( )
A.1种 B.2种 C.3种 D.4种
6.下列关于二甲苯、三甲苯、四甲苯可能具有的结构种类正确的是( )
A.3、3、3 B.3、2、2 C.3、3、4 D.3、4、3
5.有8种物质:①甲烷;②苯;③聚乙烯;④聚异戊二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯。既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是:( )
A.③④⑤⑧ B.④⑤⑦⑧ C.④⑤⑧ D.③④⑤⑦⑧
3. 下列各组物质中,所含元素的质量分数相同,但它们既不属于同分异构体,也不属于同系物的是 ( )
A.乙烯 丙烯 B.异戊二烯 3-甲基-1-丁炔
C.甲烷 乙烯 D.苯 苯乙烯
4下列说法正确的是 ( )
A. 煤的干馏是物理变化
B. 石油裂解的目的主要是为了得到更多的汽油
C. 石油分馏能得到不同沸点范围的产物
D. 石油裂化主要得到的是乙烯、丙烯等
2、下列说法正确的是( ):
A、烃的衍生物是指由烃经一步反应得到的有机生成物
B、由烃经一步反应得到的有机生成物是烃的衍生物
C、烃的衍生物中不一定有氧、氢等元素
D、卤代烃中一定有碳、氢、卤素三种元素
1.下列化学式能代表一种纯净物的是 ( )
A.C3H6 B.C5H12 C. C4H10 D.CH2Br2
第Ⅰ卷(共48分)
本卷分为第Ⅰ卷和第Ⅱ卷两部分,请将第Ⅰ卷的答案填入第Ⅱ卷中的答案题表中。考试时间100分钟,满分100分。
可能用到的原子量:C-12,O-16,H-1 Cu-64 Na-23
34.(20分)某化学反应2A  B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
|
实验序号 |
浓度(mol/L) |
时间(min) |
|||||||
|
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|||
|
1 |
温 度 |
8000C |
1.0 |
0.80 |
O.67 |
0.57 |
0.50 |
0.50 |
0.50 |
|
2 |
8000C |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
|
|
3 |
8000C |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
|
|
4 |
8200C |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在0至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度c2= mol/L,反应zai 20分钟nei就达到平衡,
可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则达到平衡时
v3 v1(填>、=、<=)且c3 = mol/L。
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。
理由是 。
(5) 800℃时,反应2A  B+D的平衡常数=
, 其他条件不变, 达到平衡时
B+D的平衡常数=
, 其他条件不变, 达到平衡时
|
32.(12分)(1)该学生用标准0.14 mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。 C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。 F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终点? 。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰
好合适”) ,原因是 。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果精确到小数点后二位)
mol/L
|
3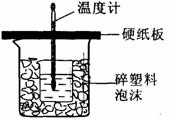 3.(8分)
(1)从实验装置上看,图中尚缺少的一种玻璃用品是
;
3.(8分)
(1)从实验装置上看,图中尚缺少的一种玻璃用品是
;
(2)由图可知该装置有不妥之处,应如何改正?
。
(3)烧杯间填满碎塑料泡沫的作用是 。
(4)大烧杯上如不盖硬纸板,则求得的中和热数值 (填“偏大”、“偏小’、“无影响”)。
(5)实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与
上述实验相比,所放出的热量 (填“相等”或“不相等”),理由
是 ;
若实验操作均正确,所求中和热的数值会 (填“相等”或“不相等”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com