
题目列表(包括答案和解析)
24.(9分)X、Y、Z是三种短周期元素,Z是自然界中原子半径最小的元素,单质
X2与Y2在放电条件下生成化合物A,X、Y、Z可以形成化合物ZXY3、XZ4XY3等。
试写出:
(1)元素X、Y、Z的元素符号分别为:X 、Y 、Z 。
(2)X2与Z2化合生成XZ3的化学方程式 。
(3)XZ3与Y2反应生成A的化学方程式 。
(4)在XZ4XY3的水溶液中,各离子浓度由大到小的顺序是 。
23.(4分)配平下列化学方程式:
KI + H2SO4(浓)= K2SO4 + SO2↑ + I2 + H2O
如反应生成1 mol I2,则电子转移的总物质的量为 mol,还原剂是 。
22.(6分)若用锌板和铜板作电极,稀硫酸为电解质溶液,制成一个原电池。试回答:
 (1)Zn板作电池的 极,发生 反应。
(1)Zn板作电池的 极,发生 反应。
Cu板上的电极反应式: 。
 (2)经过一段时间后,电解质溶液的质量 (填“变大”或“变小”)。
(2)经过一段时间后,电解质溶液的质量 (填“变大”或“变小”)。
(3)若负极质量减轻1.3 g ,则正极生成 mol气体。
21.(2分)常温下,pH = 4 的盐酸与 pH = 10 的氢氧化钠溶液等体积混合后,
溶液的 pH = (体积变化忽略不计)。
20.一定量的硝酸与 3.2 g 铜充分反应,得到的还原产物有NO2和NO。反应后溶液中含有a mol H+,则此时溶液中含有NO3- 的物质的量是
A.a mol B.(a + 0.1)mol C.0.05 mol D.无法计算
高二化学(理科)试卷
学校_______ 班级_________ 姓名________ 学号________
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Al-27 Fe-56 Cu-64 Zn-65
选择题答案表
第Ⅱ卷(非选择题 共60分)
19.在pH=1的溶液中,可以大量共存的离子组是
A.K+、Na+、SO42-、HCO3- B.Fe2+、Na+、SO42-、NO3-
C.Na+、K+、AlO2-、Cl- D.NH4+、Mg2+、SO42-、Cl-
18.体积相同、pH=3的HCl溶液和CH3COOH溶液分别跟足量的镁充分反应,则
A.HCl溶液产生较多的氢气 B.CH3COOH溶液产生较多的氢气
C.两者产生等量的氢气 D.无法比较两者产生氢气的量
17.只用一种试剂,将分别含有 Fe3+、Al3+、Mg2+、NH4+等阳离子的四种溶液区分开,这种试剂是
A.NaOH 溶液 B.NaCl 溶液 C.KSCN 溶液 D.氨水
16.下列事实不能用电化学理论解释的是
A.轮船水线以下的船壳上镶嵌有一定量的锌块
B.镀锌的铁制品比镀锡的铁制品耐腐蚀
C.铝片不用特殊方法保存
D.锌跟稀硫酸反应时,滴入少量硫酸铜溶液后反应速率加快
15.下列离子方程式书写正确的是
A.铜和稀硝酸反应 Cu + 4H+ + NO3- = Cu2+ + 2H2O + NO↑
B.碳酸氢钠的水解
HCO3- + H2O
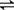 CO32- + H3O+
CO32- + H3O+
C.Fe投入盐酸中 2Fe + 6H+ = 2Fe3+ + 3H2↑
D.氢氧化铝溶于氢氧化钠溶液 Al(OH)3 + OH- = AlO2- + 2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com