
题目列表(包括答案和解析)
5.铊(81T1)是元素周期表ⅢA族元素,下列关于铊的叙述不正确的是 A.铊比铝的金属性更强 B.铊能与盐酸反应放出氢气 C.铊在化合物中可以是+3价 D.氢氧化铊一定具有两性
4.在乙烯分子中有5个σ键、一个π键,它们分别是
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键
D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键
3.当镁原子由1s22s22p63s2 →1s22s22p63p2时,以下认识正确的是
A.镁原子由基态转化成激发态,这一过程中吸收能量
B.镁原子由激发态转化成基态,这一过程中释放能量
C.转化后位于p能级上的两个电子处于同一轨道,且自旋方向相同
D.转化后镁原子与硅原子电子层结构相同,化学性质相似
2.据报道,1995年我国科研人员在兰州首次合成了镤元素的一种同位素镤-239,并测知其原子核内有148个中子。现有A元素的一种同位素,比镤-239的原子核内少54个质子和100个中子,则A元素在周期表中的位置是 A.第3周期第ⅠA族 B.第4周期第ⅠA族 C.第5周期第ⅠA族 D.第3周期第ⅡA族
1.下列关于电子云的说法中,正确的是
A.电子云表示电子在原子核外运动的轨迹
B.电子云表示电子在核外单位体积的空间出现的机会多少
C.电子云界面图中的小黑点密表示该核外空间的电子多
D.电子云可表示电子在核外运动的方向
29.(5分)炭粉和氧化铜的混合物共a g,在隔绝空气的条件下加热一段时间并冷却,固体质量变为 b g, 假设反应中炭粉全部转化为CO2,试计算:
(1)被还原的氧化铜的质量;
(2)b 的最小值。
28.(5分)向含有 0.2 mol Fe3+ 的 500 mL 溶液中加入 0.2 mol Fe 粉,充分反应,试计算:所得溶液中 Fe2+ 的物质的量浓度(假设反应前后体积不变)。
27.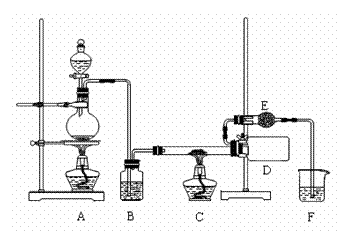 (16分)三氯化铁是一种高效、廉价的净水剂,它是红棕色固体,易潮解,100℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,装置如图所示。试回答:
(16分)三氯化铁是一种高效、廉价的净水剂,它是红棕色固体,易潮解,100℃左右时升华。实验室可用氯气与铁反应制备无水三氯化铁,装置如图所示。试回答:
(1)装置B中的试剂是 ;装置E的作用是 。
(2)反应开始时应先点燃装置 处的酒精灯,过一会儿再点燃装置 处的酒精
灯,此操作的目的是 。
(3)欲用制得的FeCl3配制溶液,应先将装置D冷却后的固体粉末溶于
(填药品名称)中,再用水稀释到所需的浓度。结合离子方程式简要说明原因
。
简述检验Fe3+的方法 。
26.(5分)某同学用标准浓度的盐酸滴定未知浓度的氢氧化钠溶液,以测定氢氧化钠
溶液的物质的量浓度。
(1)下列操作:①用标准液润洗酸式滴定管;②向酸式滴定管内注入标准液;③检查滴定管是否漏水;④滴定;⑤用水洗涤滴定管。正确的操作顺序是 。
(2)下列可能使所测氢氧化钠溶液的浓度偏低的操作是 。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.酸式滴定管在滴定前有气泡,滴定后气泡消失
C.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
D.滴定过程中,锥形瓶振荡过于剧烈,使少量溶液溅出
25.(8分)已知四种物质A、B、X、Y在一定条件下的转化关系如下图所示:

(1)若A为第三周期金属元素的单质,不与NaOH溶液反应,B为黑色固态非金属
单质,该反应的化学方程式为 。
(2)若A为第三周期金属元素的单质,可与NaOH溶液反应,X是红棕色粉末,
请写出A与NaOH溶液反应的离子方程式 。
(3)若X在常温下为无色液体,Y是具有磁性的黑色晶体,B是气态非金属单质,则
A元素在周期表中的位置为第 周期第 族,该反应的化学方程式
为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com