
题目列表(包括答案和解析)
0.5 mo1·L-1和0.2 mo1·L-1,则达到平衡后,C的浓度大于0.4 mo1·L-1
D.保持其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
第Ⅱ卷(非选择题 共60分)
15.T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图I所示;若保持其他条件不变,温度分别为Tl和T2时,B的体积百分含量与时间的关系如图Ⅱ所示。则下列结论正确的是
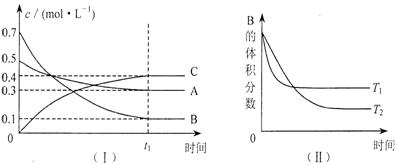

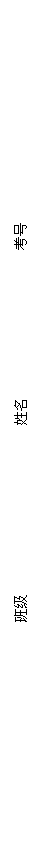
 A.在达平衡后,保持其他条件不变,增大压强,平衡向正反应方向移动
A.在达平衡后,保持其他条件不变,增大压强,平衡向正反应方向移动
B.在达平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动
C.保持其他条件不变,若反应开始时A、B、C的浓度分别为0.4mo1·L-1、
14.用质量均为100g的铜做电极,电解AgNO3溶液。电解一段时间后,两电极上的质量差为28g。则两极的质量分别为 ( ) A.阳极100g,阴极128g B.阳极93.6g,阴极121.6g C.阳极91.0g,阴极119.0g D.阳极86.0g,阴极114.0g
13.在373K 时,把0.5 mol N2O4气体通入体积为5 L(恒容)的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol·L-1。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是( )
A.前2 s,N2O4的平均反应速率为0.01 mol·L-1·s-1
B.在2 s时,体系内压强为反应前的1.1倍
C.平衡时,体系内含NO2 为0.04 mol·L-1
D.平衡时,N2O4的转化率为60%
12.在一定温度下的定容密闭容器中,当下列物理量不再变化时,不能表明反应:
A(固)+2B(气)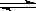 C(气)+D(气)已达平衡的是 ( )
C(气)+D(气)已达平衡的是 ( )
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.混合气体的平均分子量
11.在100mL 0.1mol/L的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是
A.加入少量Na2CO3固体 B.加入少量CH3COONa固体
C.加入少量的0.05mol/L的硫酸 D.加入少量NaCl溶液
10.25℃时,0.1mol/L的一元酸HA溶液和0.1mol/L的一元碱BOH溶液的pH之和为13,现将两溶液等体积混合,下列有关叙述中正确的是:
A.酸HA溶液的pH可能为1 B.混合溶液中c(A-)=c(B+)
C.混合溶液显碱性 D.碱BOH一定是弱碱
9.亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但遇酸性溶液发生分解:
5HClO2 → 4ClO2↑ + H+ + Cl- + 2H2O。向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反应缓慢,稍后一段时间产生气体速度较快,速度变化的原因是
A.逸出ClO2使生成物浓度降低 B.酸使亚氯酸的氧化性增强
C.溶液中的H+起催化作用 D.溶液中的Cl-起催化作用
8.25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2 800 kJ/mol,则下列热化学方程式正确的是 ( )
A.C(s)+1/2 O2(g)=CO(g) △H= - 393.5 kJ/mol
B.2H2(g)+O2(g)=2H2O(g) △H= + 571.6 kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= - 890.3 kJ/mol
D.1/2 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) △H= -1400 kJ/mol
7.一定温度下,将a mol PCl5通入一个容积不变的密闭容器中,发生反应:PCl5(g) 
PCl3(g)+Cl2(g),平衡时测得混合气体的压强为p1,此时向容器中再通入a mol PCl5,在相同温度下再次达到平衡时,测得压强为p2,下列判断正确的是 ( )
A.2p1>p2 B.PCl5的分解率增大 C.p1>p2 D.Cl2的体积分数增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com